الکتروفورز پروتئین : روش انجام آزمایش , کاربردهای بالینی و تفسیر نتایج | راهنمای جامع
الکتروفورز پروتئین یک روش آزمایشگاهی کلیدی برای جداسازی و تحلیل پروتئینهای سرم بر اساس خواص الکتریکی و فیزیکی آنها است؛ این آزمون در تشخیص و پیگیری بیماریهای ایمنی، کلیوی، کبدی و نئوپلاسمهای پلاسما نقش حیاتی دارد. در این مقاله چارچوب نظری، پروتکل عملی، الگوهای طبیعی و غیرطبیعی، نکات کنترل کیفیت و روشهای تاییدی بهصورت جامع توضیح داده شده است.
جهت عضویت در کانال آموزشی در تلگرام به لینک زیر مراجعه کنید:
https://t.me/hematology_education
فهرست مطالب
- مقدمه — اهمیت و کاربرد الکتروفورز پروتئین سرم
- اصول علمی و تئوری الکتروفورز — بار، pI و عوامل مهاجرت
- روش انجام آزمایش — پروتکل کامل عملی
- الگوی طبیعی الکتروفورز — پنج فراکسیون اصلی
- تفسیر الگوهای غیرطبیعی — مونوکلونال، پلیکلونال و …
- کنترل کیفیت و ملاحظات پیشتحلیلی
- روشهای تکمیلی و تأییدی — IFE و اندازهگیری کاپا/لامبدا آزاد
- سوالات متداول (FAQ) — ۱۰ سوال و جواب
مقدمه
الکتروفورز پروتئین سرم یکی از آزمونهای کلیدی در تشخیصهای آزمایشگاهی است که امکان جداسازی و تحلیل اجزای مختلف پروتئینهای سرم را فراهم میکند. اهمیت این آزمون از آنجاست که بسیاری از بیماریهای سیستمیک—شامل اختلالات ایمنی، بیماریهای کلیوی، کبدی، نئوپلاسمهای سلولهای پلاسما و فرآیندهای التهابی—الگوی مشخصی در این تست ایجاد میکنند. آشنایی با مبانی فیزیکوشیمیایی، اصول عملی انجام تست و تفسیر سیستماتیک الگوها، برای متخصصان آزمایشگاه و دانشجویان علوم آزمایشگاهی ضروری است.
فصل 1: اصول علمی و تئوری الکتروفورز پروتئین
1. اساس الکتروفورز
الکتروفورز فرآیندی مبتنی بر حرکت مولکولهای باردار در میدان الکتریکی است. سرعت و جهت حرکت هر مولکول به خصوصیات فیزیکوشیمیایی آن بستگی دارد. مولکولهایی با بار منفی به سمت آند و مولکولهای دارای بار مثبت به سمت کاتد حرکت میکنند. پروتئینهای سرم به دلیل ترکیب اسیدآمینهای خود در pH قلیایی دارای بار منفی شده و همگی در یک جهت حرکت میکنند، اما سرعت مهاجرت آنها متفاوت است.
2. نقش نقطه ایزوالکتریک (pI) در الکتروفورز پروتئین
پروتئینها در pH ایزوالکتریک، بار خالص صفر دارند. اگر محیط قلیاییتر از pI باشد، پروتئین بار منفی میگیرد و بالعکس. در الکتروفورز پروتئین سرم از بافر باربیتال با pH برابر 8.6 استفاده میشود که تقریباً برای تمامی پروتئینهای سرم بالاتر از pI آنهاست؛ بنابراین همگی باردار شده و در یک جهت حرکت میکنند، اما سرعت مهاجرت آنها متفاوت است.
3. عوامل مؤثر بر سرعت مهاجرت
حرکت پروتئینها در ژل تحت تأثیر مجموعهای از پارامترهاست:
- الف. بار الکتریکی — هرچه بار منفی بیشتر باشد، مولکول سریعتر حرکت میکند.
- ب. اندازه و وزن مولکولی — پروتئینهای بزرگتر مقاومت بیشتری در ماتریس ژل دارند و کندتر حرکت میکنند.
- ج. ساختار سهبعدی — پروتئینهای کمپاکت سریعتر از پروتئینهای کشیده مهاجرت میکنند.
- د. ویژگیهای محیطی — غلظت یونی بافر، ویسکوزیته، شدت میدان الکتریکی.
فصل 2: روش انجام آزمایش – پروتکل کامل و عملی
1. مواد و تجهیزات مورد نیاز برای الکتروفورز پروتئین
– دستگاه الکتروفورز افقی
– ژل آگاروز یا استات سلولز
– بافر باربیتال (pH 8.6)
– نمونه سرم غیرهمولیز
– کنترلهای نرمال و بیمار
– رنگهای اختصاصی پروتئین (آمیدو بلک، کوماسی بلو، Ponceau S)
– سیستم رنگزدایی
– آون خشککن
– دنسیتومتر و نرمافزار تحلیل باند
2. آمادهسازی نمونه
– نمونه طی ۲۴ ساعت در ۲–۸°C قابل استفاده است.
– برای نگهداری طولانی، فریز کردن در −20°C توصیه میشود.
– نمونه همولیز، لیپمیک یا ایکتریک موجب ایجاد باندهای غیرواقعی میشود.
– کلوت کامل و جدا کردن سریع سرم ضرورت دارد.
3. آمادهسازی ژل
ژل آگاروز 1% در بافر گرمشده حل میشود و روی لام شیشهای ریخته میشود. پس از سفت شدن، با کامب نمونهگذاری، چاهکها ایجاد میشوند. ضخامت یکنواخت ژل برای مهاجرت مناسب ضروری است.
4. بارگذاری نمونهها
معمولاً 3–5 µL از هر نمونه در چاهک قرار داده میشود. حجم بیش از حد باعث broadening باندها و سختی تفسیر میشود.
5. اجرای الکتروفورز
– ولتاژ: 100–150 ولت
– جریان: 40–50 mA
– زمان: حدود 30–45 دقیقه
باید دامنه دما کنترل شود؛ گرمای بیش از حد سبب پخش باندها میشود.
6. مراحل پس از الکتروفورز
الف. رنگآمیزی: ژل در رنگ پروتئین قرار داده میشود تا باندها آشکار شوند.
ب. رنگبری: بهتدریج زمینه ژل پاک و باندها واضح میشوند.
ج. خشککردن: در آون 50–60°C خشک میشود تا امکان اسکن داشته باشد.
د. اسکن و تحلیل: دنسیتومتر شدت نوری هر باند را اندازه میگیرد و مساحت زیر منحنی درصد هر فراکسیون را تعیین میکند.
فصل 3: الگوی طبیعی الکتروفورز پروتئین سرم
بهطور کلاسیک، پنج ناحیه اصلی دیده میشود:
1. آلبومین
– بزرگترین فراکسیون سرم (۵۵–۶۰٪)
– باندی باریک و قوی
– مسئول حفظ فشار انکوتیک
– کاهش آن اغلب نشانه بیماری سیستمیک است
2. آلفا-1 گلوبولین
– ۲–۴٪
– شامل آلفا-1 آنتیتریپسین و آلفا-1 اسید گلیکوپروتئین
– افزایش در التهاب حاد
– کاهش در کمبود آلفا-1 آنتیتریپسین
3. آلفا-2 گلوبولین
– ۶–۸٪
– شامل هاپتوگلوبین، آلفا-2 ماکروگلوبولین، سرولوپلاسمین
– افزایش مشخص در سندرم نفروتیک
4. بتا گلوبولین
– ۹–۱۳٪
– شامل ترانسفرین، کمپلمان C3، بتا-لیپوپروتئین
– ناحیهای که ممکن است باندهای مونوکلونال پنهان در آن ظاهر شوند
5. گاما گلوبولین
– ۱۱–۱۸٪
– عمدتاً متشکل از IgG, IgA, IgM
– الگوی طبیعی پلیکلونال است
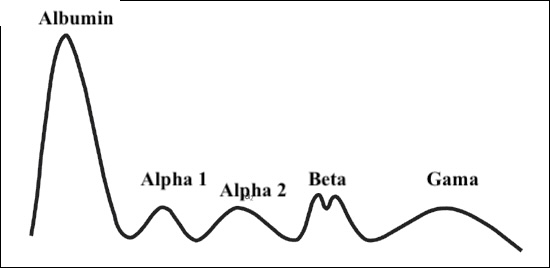
الکتروفورز پروتئین
فصل 4: تفسیر الگوهای غیرطبیعی الکتروفورز هموگلوبین
1. الگوی مونوکلونال (M-Spike)
مشخصه آن وجود یک باند باریک، تیز و واضح است. مکان ظهور باند میتواند در گاما، بتا یا حتی آلفا-2 باشد.
بیماریهای مرتبط:
– مولتیپل میلوما
– MGUS
– ماکروگلوبولینمی والدنشتروم
– آمیلوئیدوز AL
– برخی لوسمیهای لنفویید
2. افزایش پلیکلونال گاما
باند پهن و منتشر به علت تحریک ایمنی گسترده.
بیماریهای مرتبط:
– عفونتهای مزمن
– بیماریهای خودایمنی
– بیماریهای کبدی
– سارکوئیدوز
3. الگوی سندرم نفروتیک
– کاهش شدید آلبومین
– افزایش آلفا-2
– کاهش گاما
علت آن از دست دادن آلبومین از کلیه و افزایش جبرانی آلفا-2 ماکروگلوبولین است.
4. الگوی سیروز کبدی
– آلبومین پایین
– افزایش گاما
– تشکیل پل بین بتا و گاما (Beta-Gamma Bridging)
– کاهش آلفا-1 و آلفا-2
5. الگوی التهاب حاد
– کاهش آلبومین
– افزایش آلفا-1 و آلفا-2
– افزایش پروتئینهای فاز حاد مانند CRP
فصل 5: کنترل کیفیت، خطاهای پیشتحلیلی و محدودیتهای الکتروفورز پروتئین
کنترل کیفیت
– استفاده از کنترلهای نرمال و پاتولوژیک در هر ران
– رسم نمودارهای QC و تحلیل روندها
– پایش ولتاژ، بافر، ژل و زمان اجرا
نکات مهم پیشتحلیلی
– نمونهگیری غیرناشتا میتواند لیپمی ایجاد کند.
– تأخیر در جدا کردن سرم باندهای کاذب ایجاد میکند.
– همولیز باعث باند هموگلوبین میشود و تفسیر را مختل میکند.
محدودیتهای روش
– تشخیص باندهای مونوکلونال کوچک با حساسیت پایین
– عدم توانایی در تعیین نوع زنجیرههای سنگین و سبک
– وابستگی به تجربه متخصص تفسیرکننده
– حساسیت پایینتر در مقایسه با IFE
فصل 6: روشهای تکمیلی
1. ایمونوفیکساسیون (IFE)
استاندارد طلایی برای تشخیص و تایپ پروتئینهای مونوکلونال — تعیین زنجیره سنگین و سبک — حساستر از الکتروفورز معمولی.
2. سنجش کاپا/لامبدا آزاد
برای پایش پاسخ به درمان در مولتیپل میلوما ضروری است، بهویژه در بیماران با میلوماهای زنجیره سبک.
جمعبندی الکتروفورز پروتئین
الکتروفورز پروتئین سرم روشی کلیدی، قابل اتکا و نسبتاً ارزان در تشخیص آزمایشگاهی است. درک اصول علمی، اجرای دقیق مراحل عملی، توجه به خطاهای پیشتحلیلی و کنترل کیفیت، و بهکارگیری روشهای تأییدی مانند ایمونوفیکساسیون برای تفسیر صحیح نتایج ضروری است. بسیاری از بیماریهای مهم داخلی، ایمنی، کبدی و خون در این آزمون الگوهای مشخصی ایجاد میکنند، و تفسیر درست آن نقش مهمی در تصمیمگیری تشخیصی و درمانی دارد.
نکته عملی و مدیریتی
توجه به کنترل کیفیت، ملاحظات پیشتحلیلی و استفاده به موقع از روشهای تأییدی، دقت و صحت نتایج این آزمایش مهم را تضمین میکند.
سوالات رایج (FAQ) در مورد الکتروفورز پروتئین
۱) الکتروفورز پروتئین چیست و چه کاربردهایی دارد؟
الکتروفورز پروتئین روشی برای جداسازی پروتئینها بر اساس بار و اندازه است. در تشخیص بیماریهای ایمنی، بیماریهای کلیوی، کبدی و نئوپلاسمهای پلاسما کاربرد دارد.
۲) چه تفاوتی بین الکتروفورز معمولی و ایمونوفیکساسیون وجود دارد؟
الکتروفورز برای جداسازی کلی فراکسیونها استفاده میشود؛ ایمونوفیکساسیون (IFE) روش تاییدی و حساستری است که نوع زنجیرههای سنگین و سبک را شناسایی میکند.
۳) نمونهها چگونه باید نگهداری شوند؟
نمونه تا ۲۴ ساعت در ۲–۸°C پایدار است. برای نگهداری طولانیتر در −20°C فریز کنید. از همولیز یا لیپمیک بودن نمونه خودداری کنید.
۴) یک باند تیز در ناحیه گاما به چه معناست؟
وجود یک باند تیز میتواند نشاندهنده پروتئین مونوکلونال باشد؛ ممکن است مربوط به مولتیپل میلوما، MGUS یا سایر اختلالات پلاسماسل باشد و نیاز به تایید با IFE دارد.
۵) الگوی پلیکلونال نشاندهنده چه چیزی است؟
افزایش منتشر و پهن در ناحیه گاما که معمولاً به علت پاسخ ایمنی گسترده در عفونتهای مزمن، بیماریهای خودایمنی یا بیماریهای کبدی ایجاد میشود.
۶) آیا الکتروفورز میتواند نوع ایمونوگلوبولین را تعیین کند؟
خیر؛ الکتروفورز معمولی نوع زنجیره را تعیین نمیکند — برای این کار باید از ایمونوفیکساسیون استفاده کرد.
۷) چه عواملی میتواند در تفسیر نتایج اختلال ایجاد کند؟
همولیز، لیپمی، تأخیر در جدا کردن سرم، پرفشار بودن بافر و اجرای نادرست الکتروفورز میتوانند باندهای کاذب یا پخش باند ایجاد کنند.
۸) چه زمانی باید IFE درخواست دهیم؟
وقتی یک باند مونوکلونال در الکتروفورز دیده شود یا شکی به وجود یک پروتئین مونوکلونال باشد، برای تعیین تیپ ایمونوگلوبولین و زنجیره سبک درخواست IFE ضروری است.
۹) آیا الکتروفورز برای پایش درمان مناسب است؟
الکتروفورز میتواند در پایش تغییرات باندهای مونوکلونال مفید باشد، اما برای ارزیابی دقیقتر پاسخ به درمان اغلب از سنجش زنجیرههای سبک آزاد استفاده میشود.
۱۰) چه محدودیتهایی در حساسیت الکتروفورز وجود دارد؟
الکتروفورز حساسیت محدودی برای پروتئینهای مونوکلونال با بار کم دارد و ممکن است باندهای کوچک را نشان ندهد؛ در چنین مواردی IFE یا تستهای حساستر لازم است.
منابع معتبر برای مطالعه بیشتر در مورد الکتروفورز پروتئین
