رنگ آمیزی ایمونوهیستوشیمی (Immunohistochemistry; IHC): اصول، اجرا، تفسیر و کنترل کیفیت
فهرست مطالب
خلاصه
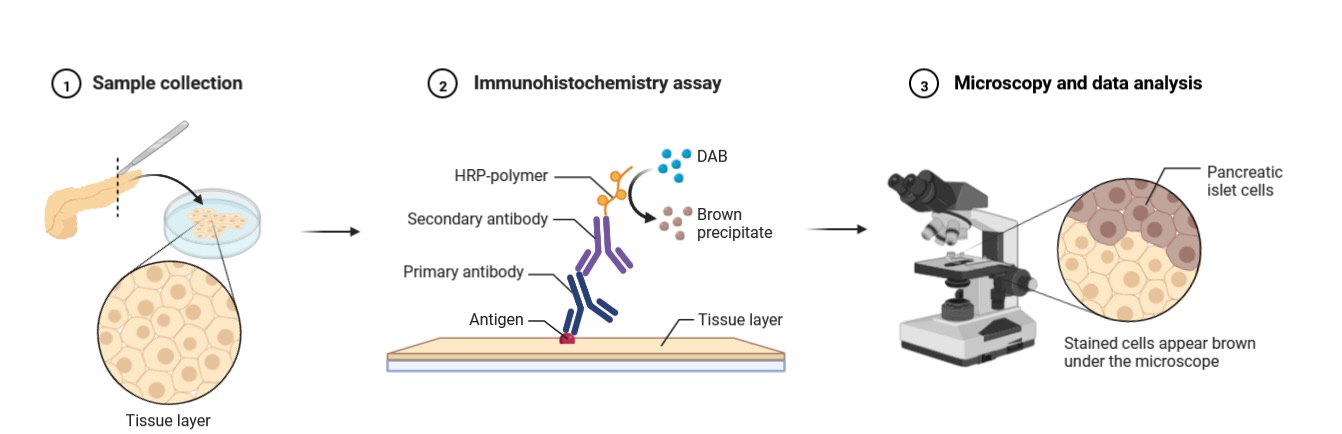
رنگ آمیزی ایمونوهیستوشیمی (Immunohistochemistry; IHC) تکنیکی است که با استفاده از اتصال اختصاصی آنتیبادی به اپیتوپ، امکان شناسایی، مکانیابی و نیمهکمیسازی پروتئینها در بافتهای فیکسشده را فراهم میکند؛ این مقاله اصول، پروتکل کامل FFPE، معیارهای تفسیر و چارچوب کنترل کیفیت را در قالب یک راهنمای عملی و بهروز ارائه میدهد.
مقدمه رنگ آمیزی ایمونوهیستوشیمی
رنگ آمیزی ایمونوهیستوشیمی بهعنوان یکی از مهمترین ابزارهای تشخیصی در پاتولوژی آناتومیک شناخته میشود. این تکنیک امکان ارزیابی همزمان مورفولوژی سلولی و بیان پروتئینی را در بافت فراهم میکند و برخلاف روشهای مولکولی استخراجی (مانند Western blot یا RT-PCR)، اطلاعات مکانی («در کدام سلول و در کدام کمپارتمان سلولی») را حفظ میکند. اساس روش بر اتصال اختصاصی آنتیبادی اولیه به اپیتوپ هدف و سپس آشکارسازی این اتصال از طریق سیستمهای آنزیمی یا فلوئورسنت استوار است. کروموژن رایج دیآمینوبنزیدین (DAB) رسوب قهوهای پایدار ایجاد میکند که با میکروسکوپ نوری قابل مشاهده است.
اصول بنیادی رنگ آمیزی ایمونوهیستوشیمی
سه اصل کلیدی موفقیت IHC:
- اختصاصیت و میل ترکیبی بالای واکنش آنتیژن-آنتیبادی
- بازیابی آنتیژن (Antigen Retrieval; AR) برای رفع ماسکه شدن اپیتوپها ناشی از فیکساسیون فرمالین
- سیستمهای آشکارسازی حساس و بدون بیوتین (سیستمهای پلیمری نسل جدید امروزه استاندارد طلایی هستند)
کاربردهای بالینی رنگ آمیزی ایمونوهیستوشیمی
الف) تشخیص افتراقی و تعیین منشأ تومورهای متاستاتیک ناشناخته (CUP)
– پانلهای تشخیصی برای کارسینوم ناشناخته: CK7/CK20/CDX2/TTF1/PSA/GATA3
– پانلهای تومورهای گردوند (round cell tumors): CD45/CD3/CD20/CD79a/PAX5/TdT
– پانلهای سارکوم: Vimentin/Desmin/SMA/S100/CD31
ب) طبقهبندی مولکولی تومورها
– طبقهبندی لنفوم: CD20/CD3/CD5/CD10/BCL2/BCL6/Ki-67/MUM1
– زیرگروهبادی کارسینوم پستان: ER/PR/HER2/Ki-67
– طبقهبندی تومورهای ریه: TTF1/p40/Napsin A/CK7
ج) مارکرهای پیشآگهی
– شاخص پرولیفراسیون: Ki-67 در تومورهای نورواندوکراین، لنفوم، سارکوم
– مارکرهای آپوپتوز: BCL2 در لنفوم فولیکولار
– مارکرهای آنژیوژنز: CD31/CD34 در آنژیوسارکوم
د) مارکرهای پیشبینیکننده پاسخ درمانی
– گیرنده استروژن و پروژسترون (ER/PR) در پستان
– HER2 در پستان و معده
– PD-L1 (TPS/CPS) در ریه، ملانوم، مثانه
– dMMR/MSI در کولون و آندومتر
– ALK/ROS1/BRAF/NTRK در ریه و تومورهای جامد
– TMB-H در انواع تومورها
پروتکل عملی رنگ آمیزی ایمونوهیستوشیمی (IHC) روی بافت FFPE – نسخهٔ کامل و دقیق آزمایشگاهی (استاندارد NordiQC/CAP/NEQAS ۲۰۲۵)
۱. برشگیری (sectioning)
– ضخامت برش: ۳–۴ میکرون (مارکرهای هستهای مانند Ki-67, ER, PR → ۳ میکرون؛ مارکرهای غشایی مانند HER2 → تا ۴ میکرون)
– لام: شارژدار (positively charged) یا سیلاندار (Superfrost Plus یا Poly-L-Lysine coated)
– خشک کردن: ۶۰–۶۵°C به مدت حداقل ۱ ساعت (ترجیحاً یک شب)
۲. دپارافینیزاسیون و ریهیدراسیون (deparaffinization and rehydration)
| مرحله | محلول | زمان | دما |
|---|---|---|---|
| زایلن I | زایلن تازه | ۱۰ دقیقه | اتاق |
| زایلن II | زایلن تازه | ۱۰ دقیقه | اتاق |
| زایلن III | زایلن تازه | ۵ دقیقه | اتاق |
| الکل مطلق I | ۱۰۰٪ | ۳ دقیقه | اتاق |
| الکل مطلق II | ۱۰۰٪ | ۳ دقیقه | اتاق |
| الکل ۹۵٪ | — | ۳ دقیقه | اتاق |
| الکل ۸۰٪ | — | ۳ دقیقه | اتاق |
| الکل ۷۰٪ | — | ۳ دقیقه | اتاق |
| آب مقطر | — | ۳ دقیقه × ۲ | اتاق |
۳. بازیابی آنتیژن (Antigen Retrieval) – مهمترین مرحله رنگ آمیزی ایمونوهیستوشیمی
الف) بازیابی حرارتی (HIER – Heat-Induced Epitope Retrieval)
| بافر | pH | دما و زمان پیشنهادی | مثال مارکرها |
|---|---|---|---|
| سیترات | ۶.۰ | ۱۲۵°C × ۳ دقیقه + ۱۰–۲۰ دقیقه خنکسازی طبیعی (Pressure cooker یا PT-Link) | CK7, CK20, CDX2, TTF-1, PAX8, Synaptophysin |
| EDTA یا Tris-EDTA | ۹.۰ | همان | CD3, CD4, CD8, CD20, Ki-67, ER, PR, PD-L1, HER2, ALK |
نکته: (بازیابی حرارتی / Heat-Induced Epitope Retrieval; HIER). پس از اتمام زمان فشار، درب باز نشود تا فشار کاملاً بیفتد؛ سپس ۱۵–۲۰ دقیقه در بافر خنک شود.
ب) بازیابی آنزیمی
فقط موارد خاص: پپسین ۰.۴٪ یا Proteinase K، ۵–۱۵ دقیقه در ۳۷°C
۴. مهار پراکسیداز اندوژن
۳٪ هیدروژن پراکسید (H₂O₂) در متانول یا آب مقطر، ۱۰–۱۵ دقیقه در تاریکی
شستشو: ۳ بار × ۳ دقیقه در PBS/TBS
۵. بلوکینگ غیراختصاصی (non-specific blocking)
پروتئینبلوک یا سرم نرمال ۱۰٪، ۱۰–۲۰ دقیقه در دمای اتاق؛ مایع اضافی تخلیه شود
۶. انکوباسیون آنتیبادی اولیه
| نوع انکوباسیون | زمان پیشنهادی | دما | مثال مارکرها |
|---|---|---|---|
| یک شبه (Overnight) | ۱۶–۱۸ ساعت | ۴°C (یخچال) | Ki-67, ER, PR, PAX8, PD-L1, HER2, ALK |
| کوتاه | ۳۰–۶۰ دقیقه | اتاق/۳۷°C | CK7, CK20, CD20, Chromogranin, S100 |
حجم: ۱۰۰–۲۰۰ میکرولیتر؛ حتماً در humidity chamber
۷. انکوباسیون سیستم آشکارسازی
سیستمهای پلیمری بدون بیوتین (استاندارد طلایی): EnVision™ FLEX │ UltraView │ Bond Polymer Refine │ Mach 4
زمان معمول: ۲۰–۳۲ دقیقه
۸. آشکارسازی کروموژنیک
DAB: ۵–۸ دقیقه (کنترل میکروسکوپی) → شستشو با آب مقطر
۹. کانتراستین (counterstaining)
هماتوکسیلین مایر ۳۰–۶۰ ثانیه یا هریس ۱–۲ دقیقه → آب جاری ۵ دقیقه
۱۰. دهیدراتاسیون و مانتینگ (mounting)
الکل ۷۰→۸۰→۹۵→مطلق I→مطلق II → زایلن I و II → مانت با Entellan/DPX/Permount
نکات طلایی عملی:
- بافرهای بازیابی هر روز تازه تهیه شود
- هر ۱۰–۱۵ نمونه یک کنترل مثبت خارجی روی همان ران
- دمای Pressure cooker با ترمومتر کالیبره شود
- مارکرهای حساس (CD5, Cyclin D1, CD4) حتماً یک شبه در ۴°C
- DAB کارسینوژن → در هود و با دستکش
- همیشه humidity chamber
معیارهای تفسیر رنگ آمیزی ایمونوهیستوشیمی
– محل رنگآمیزی: هستهای، غشایی، سیتوپلاسمی یا ترکیبی
– شدت: ۰, ۱+, ۲+, ۳+
– گستردگی: درصد سلولهای توموری مثبت
– سیستمهای نمرهدهی استاندارد: HER2 (ASCO/CAP ۲۰۱۸/۲۰۲۳)، ER/PR (Allred/H-score)، PD-L1 (TPS/CPS/IC)، Ki-67 (درصد)
کنترل کیفی رنگ آمیزی ایمونوهیستوشیمی
الف) کنترل داخلی
– کنترل مثبت داخلی: سلولهای طبیعی در همان بافت که باید واکنش مشخصی نشان دهند
– کنترل منفی داخلی: سلولهایی که نباید رنگ بگیرند
ب) کنترل خارجی
– کنترل مثبت خارجی: بافتهای TMA حاوی نمونههای مثبت شناخته شده
– کنترل منفی خارجی: بافت مشابه بدون آنتیبادی اولیه
ج) کنترل فنی
– کنترل حذف آنتیبادی اولیه
– کنترل سیستم آشکارسازی
– کنترل بازیابی آنتیژن
د) برنامههای تضمین کیفیت خارجی
– مشارکت اجباری در برنامههای بینالمللی: NordiQC, UK NEQAS, CAP Surveys
– بازرسی دورهای و ممیزی داخلی
– کالیبراسیون دورهای دستگاهها و بافرها
ه) مستندسازی
– ثبت کلیه پارامترهای آزمایش شامل: batch آنتیبادی، زمان انکوباسیون، شرایط بازیابی آنتیژن
– ثبت و پیگیری نتایج کنترلهای کیفی
راهنمای عیبیابی (Troubleshooting) رنگ آمیزی ایمونوهیستوشیمی
الف) رنگآمیزی ضعیف یا منفی در رنگ آمیزی ایمونوهیستوشیمی
علل احتمالی:
- بازیابی آنتیژن ناکافی (pH یا زمان نادرست)
- آنتیبادی اولیه رقیقشده یا فعالیت از دست رفته
- زمان انکوباسیون ناکافی
- سیستم آشکارسازی خراب
راه حل:
- بهینهسازی شرایط بازیابی آنتیژن
- تیتراسیون مجدد آنتیبادی
- افزایش زمان انکوباسیون
- استفاده از کنترل مثبت
ب) رنگآمیزی غیراختصاصی یا پسزمینه بالا
علل احتمالی:
- بلوکینگ ناکافی (بلوکینگ غیراختصاصی / non-specific blocking)
- شستشوی ناکافی
- غلظت بالای آنتیبادی
- endogenous enzyme activity
راه حل:
- بهینهسازی زمان و ماده بلوکینگ
- افزایش دفعات و زمان شستشو
- رقیقسازی آنتیبادی
- اطمینان از مهار کامل پراکسیداز/آلکالین فسفاتاز
ج) رنگآمیزی لکهای یا ناهمگن
علل احتمالی:
- خشک شدن سطح بافت حین انکوباسیون
- عدم پوشش یکنواخت آنتیبادی
- وجود حباب هوا
راه حل:
- استفاده از humidity chamber
- اطمینان از پوشش کامل سطح بافت
- حذف حبابهای هوا
د) رنگآمیزی شدید یا overstaining
علل احتمالی:
- غلظت بالای آنتیبادی
- زمان طولانی انکوباسیون با DAB
- دمای بالای انکوباسیون
راه حل:
- رقیقسازی آنتیبادی
- کاهش زمان انکوباسیون با کروموژن
- کنترل دمای انکوباسیون
نتیجهگیری
رنگ آمیزی ایمونوهیستوشیمی همچنان قابلاعتمادترین و پرکاربردترین تکنیک در پاتولوژی تشخیصی است. دقت نتایج مستقیماً وابسته به رعایت دقیق پروتکل، استفاده از آنتیبادیهای معتبر، تفسیر توسط پاتولوژیست مجرب و اجرای برنامه سختگیرانه کنترل کیفیت است. با ظهور سیستمهای پلیمری نسل جدید و مارکرهای همراه تشخیصی جدید، نقش IHC در پزشکی دقیق روزبهروز حیاتیتر میشود.
سوالات رایج (FAQ) در مورد رنگ آمیزی ایمونوهیستوشیمی
۱) رنگ آمیزی ایمونوهیستوشیمی (IHC) دقیقاً چه اطلاعاتی به ما میدهد؟
IHC محل دقیق بیان پروتئینها را در بافت نشان میدهد (هستهای، سیتوپلاسمی یا غشایی)، بنابراین علاوه بر وجود یا عدم وجود یک مارکر، توزیع سلولی و مقدار تقریبی آن قابل مشاهده است.
۲) چرا بازیابی آنتیژن (Antigen Retrieval) در رنگ آمیزی ایمونوهیستوشیمی انجام میشود و چه انواعی دارد؟
فیکساسیون با فرمالین باعث ماسکه شدن اپیتوپها میشود؛ بازیابی آنتیژن (AR) اپیتوپها را باز میکند. دو روش متداول وجود دارد: بازیابی حرارتی (HIER – Heat-Induced Epitope Retrieval) و بازیابی آنزیمی (Enzymatic retrieval).
۳) کنترل مثبت و کنترل منفی در رنگ آمیزی ایمونوهیستوشیمی چگونه باید استفاده شوند؟
کنترل مثبت باید بافتی باشد که به طور معتبر مارکر مورد نظر را نشان میدهد؛ کنترل منفی میتواند شامل حذف آنتیبادی اولیه باشد. همچنین کنترلهای داخلی در همان اسلاید بسیار کمککنندهاند.
۴) علت بروز پسزمینه (background) بالا چیست و چگونه آن را کاهش دهیم؟
علل شامل بلوکینگ ناکافی، غلظت بالای آنتیبادی یا عدم شستشوی کاملاند. راهکارها: افزایش بلوکینگ (non-specific blocking)، کاهش غلظت آنتیبادی، و افزایش دفعات شستشو.
۵) چه زمانی باید از DAB استفاده کنیم و چه خطراتی دارد؟
DAB یک کروموژن رایج برای میکروسکوپ نوری است و رسوب قهوهای پایداری ایجاد میکند؛ اما DAB کارسینوژن است، بنابراین استفاده در زیر هود و با حفاظت مناسب ضروری است.
۶) تفاوت بین انکوباسیون یک شبه و کوتاه چیست و چه مواقعی استفاده میشود؟
انکوباسیون یک شبه در ۴°C مناسب مارکرهای حساس و با آنتیبادیهای ضعیف است؛ انکوباسیون کوتاه در دمای اتاق یا ۳۷°C برای مارکرهای قویتر یا زمانی که تایم محدود دارید استفاده میشود.
۷) چگونه شدت (intensity) و گستردگی (extent) را نمرهدهی کنیم؟
شدت معمولاً ۰ تا ۳+ و گستردگی بهصورت درصد سلولهای مثبت گزارش میشود. برای برخی مارکرها (مانند HER2, ER/PR, PD-L1) سیستمهای نمرهدهی استاندارد وجود دارد (ASCO/CAP، Allred، TPS/CPS).
۸) آیا نتایج IHC نیاز به تایید با روش مولکولی دارند؟
بستگی به مارکر و کاربرد بالینی دارد؛ در برخی موارد (مثلاً ALK, ROS1, NTRK) تایید مولکولی (FISH/NGS) ممکن است لازم یا توصیه شود، مخصوصاً در موارد درمان هدفمند.
۹) چه نکاتی برای نگهداری آنتیبادیها و بافرها در رنگ آمیزی ایمونوهیستوشیمی مهم است؟
آنتیبادیها را مطابق توصیه سازنده نگهداری کنید (برای مثال در -20°C یا 4°C بسته به نوع) و بافرهای بازیابی را روزانه تازه آماده کنید تا از آلودگی و کاهش کارایی جلوگیری شود.
۱۰) چگونه کیفیت آزمایشگاه IHC را بهبود دهیم؟
اجرای برنامه کنترل کیفیت داخلی و خارجی (شرکت در NordiQC، UK NEQAS، CAP)، کالیبراسیون تجهیزات، آموزش مداوم پرسنل، و مستندسازی دقیق پارامترهای آزمایش از کلیدهای بهبود کیفیت هستند.
منابع رنگ آمیزی ایمونوهیستوشیمی
- Dabbs DJ. Diagnostic Immunohistochemistry, 6th ed. Elsevier 2022
- Taylor CR, Rudbeck L. Immunohistochemical Staining Methods, 7th ed. Agilent 2020
- Wolff AC et al. HER2 Testing in Breast Cancer: ASCO/CAP Guideline 2018 & 2023 addendum
- NordiQC Guidelines & Assessment Runs (تا Run ۷۱, ۲۰۲۵)
- College of American Pathologists (CAP) Immunohistochemistry Committee Guidelines
- Ramos-Vara JA & Miller MA. Immunohistochemistry: Essential Elements and Beyond. Vet Pathol 2024
منابع آنلاین مرتبط با رنگ آمیزی ایمونوهیستوشیمی
