راهنمای جامع کنترل کیفی بیوشیمی (IQC/EQA) با قوانین Westgard
کنترل کیفی بیوشیمی مجموعهای از روشهای آماری و اجرایی برای تضمین صحت (Accuracy)، دقت و تکرارپذیری (Precision) نتایج در بخش بیوشیمی است. استقرار اصولیِ IQC و EQA، تفسیر قوانین Westgard و مستندسازی کامل سبب میشود خطاهای تصادفی و سیستماتیک پیش از اثرگذاری بر گزارش بیماران شناسایی شوند و الزامات استانداردهایی مانند ISO 15189 نیز پوشش داده شوند.
جهت عضویت در کانال آموزشی تلگرام از لینک زیر استفاده کنید:
🚀 عضویت در کانال تلگرام
فهرست مطالب
مقدمه ی کنترل کیفی بیوشیمی
کنترل کیفی بیوشیمی ستون فقرات نظام تضمین کیفیت آزمایشگاه است. چون بخش چشمگیری از تصمیمهای بالینی بر پایهی نتایج بیوشیمی اتخاذ میشود، حتی انحرافهای کوچک میتواند به تشخیص نادرست، درمان نامتناسب یا تغییر مسیر درمان بینجامد. هدف QC صرفاً پیدا کردن خطا نیست؛ بلکه ایجاد فرهنگ دقت، پایش پیوسته و پیشگیری از خطا در تمام مراحل فرآیند آزمایش است.
در بیوشیمی، آزمونهایی مانند گلوکز، اوره، کراتینین، آنزیمهای کبدی، پروفایلهای لیپیدی و الکترولیتها هر روز برای بیماران متعدد انجام میشود و به کیفیت معرف، وضعیت کالیبراسیون و مهارت اپراتور وابستگی شدیدی دارند؛ بنابراین اجرای دقیق QC حیاتی است.
برای مطالعهی کنترل کیفی در سایر بخشها به لینک های زیر مراجعه کنید:
هماتولوژی |
میکروبشناسی |
ادرار
اهداف کنترل کیفی بیوشیمی
- تضمین صحت و دقت نتایج (Accuracy & Precision): نتایج باید هم به مقدار واقعی نزدیک باشند و هم در تکرارها پایداری نشان دهند.
- کشف زودهنگام خطاهای سیستماتیک و تصادفی: پیش از آنکه به گزارش بیمار راه یابند.
- افزایش اعتماد ذینفعان: آزمایشگاهی که QC منظم و مستند دارد، در ارزیابیها و ممیزیها جایگاه مطلوبتری مییابد.
یک موقعیت واقعی: اگر در چند روز متوالی نتایج گلوکز حدود ۱۰٪ بالاتر از الگوی معمول ثبت شود، بدون QC احتمال برداشت نادرست از کنترل دیابت وجود دارد؛ QC فعال چنین تغییراتی را پیش از گزارش آشکار میکند.
مفاهیم آماری پایه (Mean، SD، CV، Bias)
میانگین (Mean)
میانگین نمایندهی مقدار مرکزی دادههاست و مبنای تحلیل QC برای سریهای متوالی اندازهگیری محسوب میشود.
نمونه: ۲۰ اندازهگیری کنترل گلوکز با میانگین ≈ 100 mg/dL.
انحراف معیار (Standard Deviation – SD)
SD میزان پراکندگی نتایج پیرامون میانگین را نشان میدهد؛ هرچه SD کمتر، پایداری بیشتر.
فرمول: SD = √[Σ(x−x̄)² / (n−1)]
نمونه: اوره 29، 30، 31، 30، 29 → SD ≈ 0.89 (بسیار مطلوب).
ضریب تغییرات (Coefficient of Variation – CV%)
CV = (SD/Mean)×100؛ برای مقایسهی نسبی پایداری در آزمونهای گوناگون.
| تست | CV قابل قبول |
|---|---|
| گلوکز | < 3% |
| اوره، کراتینین | < 5% |
| الکترولیتها (Na⁺, K⁺) | < 2% |
| آنزیمها (ALT, AST) | < 6% |
نمونه: Mean ALT=45، SD=2.7 → CV=6% → قابل قبول اما در آستانهی هشدار.
بایاس (Bias)
اختلاف میانگین نتایج آزمایشگاه با مقدار مرجع را نشان میدهد.
Bias = (Mean_lab − Mean_ref) / Mean_ref × 100
نمونه: Mean_lab=105، Mean_ref=100 → Bias=+5%.
خطاهای تصادفی و سیستماتیک در کنترل کیفی بیوشیمی
| نوع خطا | ویژگی | مثال | راهکار |
|---|---|---|---|
| تصادفی | غیرقابل پیشبینی و نوسانی | حباب در پیپت، نوسان دما | تکرار تست، کنترل ابزار |
| سیستماتیک | جهتدار و مداوم | کالیبراسیون نادرست، معرف فاسد | تنظیم مجدد، تعویض معرف |
محدوده مجاز (Control Range)
برای کنترل جدید، حداقل ۲۰ بار در شرایط پایدار اندازهگیری کنید تا Mean و SD واقعی تعیین شود. محدودهی مجاز = Mean ± 2SD.
نمونه: Mean=100 و SD=1.5 → بازهی 97 تا 103. اگر در روز ۲۵ مقدار 104.5 ثبت شد، هشدار قانون 1 2s فعال میشود.
ثبت و نگهداری دادههای QC
فرم یا فایل دیجیتال باید این موارد را داشته باشد: تاریخ/شیفت، نام اپراتور، دستگاه، سری معرف/کنترل، سطح کنترل (Low/Normal/High)، نتیجه، محدودهی مجاز، تفسیر (قبول/رد) و اقدام اصلاحی.
کنترل کیفی داخلی (IQC) – چارچوب و مراحل
IQC با استفاده از نمونههای کنترل با غلظت مشخص انجام میشود تا اطمینان حاصل کنیم دستگاه و معرف در شرایط معمول عملکرد صحیح دارند. IQC در حکم آژیر هشدار روزانه پیش از شروع کار بیماران است.
مراحل اجرای IQC
- انتخاب سرم کنترل: ماتریکس مشابه سرم انسانی، پایداری پس از بازشدن (۷ روز در ۲–۸°C)، وجود سطوح Low/Normal/High و سازگاری با روش/دستگاه.
- آمادهسازی کنترل لیوفیلیزه: بازسازی طبق دستور سازنده، پرهیز از vortex شدید، همدماسازی ~۱۰ دقیقه در دمای اتاق، انجام فوری تست یا نگهداری در ۲–۸°C.
- استقرار محدودههای پذیرش: حداقل ۲۰ اندازهگیری برای کنترل جدید در روزهای مختلف؛ نمونه: کراتینین Mean=1.00 mg/dL، SD=0.05 → محدوده 0.90–1.10.
- رسم Levey–Jennings: محور افقی روز و محور عمودی مقدار کنترل؛ خطوط Mean، ±1SD، ±2SD، ±3SD. الگوی نقطهها، ثبات، Bias یا نوسان را نشان میدهد.
قوانین Westgard در کنترل کیفی بیوشیمی با مثالهای عددی
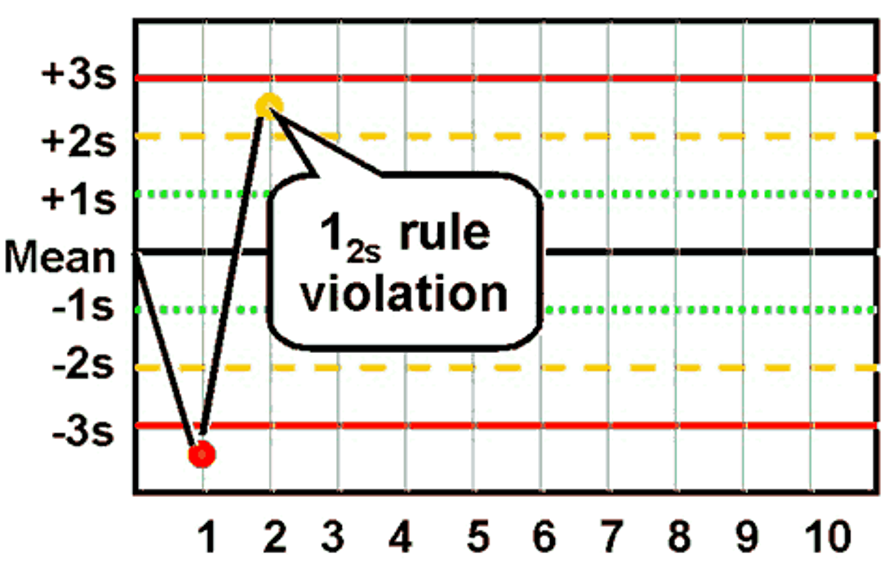
🔹 قانون 1 2s — هشدار اولیه
اگر یک نقطهی کنترل خارج از ±2SD باشد، هشدار فعال است اما الزاماً مردودی قطعی نیست.
نمونه: Mean=100، SD=2، نتیجه=104.5 → 2.25SD.
اقدام: تکرار کنترل؛ اگر دوباره خارج از محدوده بود، بررسی ادامه یابد.
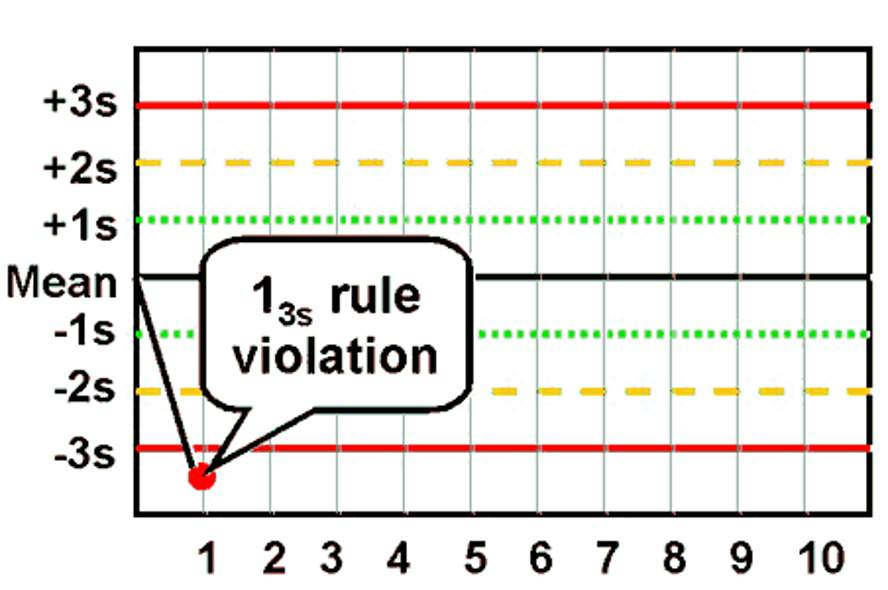
🔹 قانون 1 3s — رد فوری سری
خروج هر نقطه از ±3SD نشانگر خطای جدی است.
نمونه: Mean=100، SD=2، مقدار=107 → 3.5SD.
اقدام: تکرار؛ در صورت تأیید، تاریخ معرف، تمیزی کووت و دمای انکوباتور بررسی شود.
🔹 قانون 2 2s — خطای سیستماتیک
دو نتیجهی متوالی یا دو سطح در یک جهت و هر دو فراتر از ±2SD.
تفسیر: Bias پایدار محتمل است.
اقدام: بازبینی کالیبراسیون، حجمدهی نمونه/معرف، وضعیت اپتیک/لامپ.
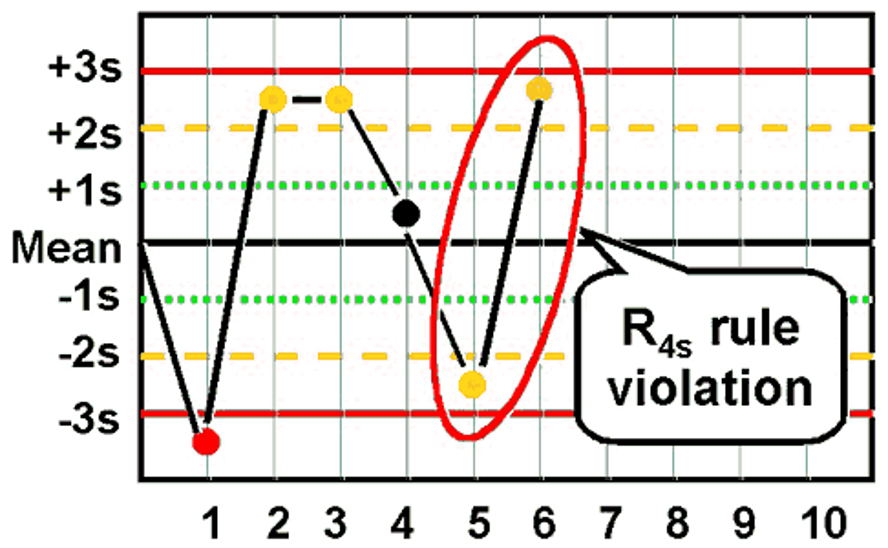
🔹 قانون R 4s — خطای تصادفی
اختلاف بین دو کنترل در یک سری بیش از 4SD باشد.
تفسیر: خطای تصادفی (پیپتینگ، حباب، نوسان دما).
اقدام: تکرار هر دو کنترل و بررسی ابزار.
🔹 قانون 4 1s — سیستماتیک بلندمدت
چهار نتیجهی متوالی در یک سمتِ ±1SD نشانگر Drift تدریجی است.
اقدام: بررسی دمای انکوباتور، پمپها و احتمال نیاز به کالیبراسیون.
🔹 قانون 10x — بایاس مزمن
ده نتیجهی پیاپی در یک طرف Mean (همگی بالا یا همگی پایین).
اقدام: ریشهیابی Bias و اجرای اصلاح اساسی (کالیبراسیون/معرف).
🔹 قانون 2 of 3 2s — قانون ترکیبی
از سه نتیجهی متوالی، دو نتیجه در یک جهت و هر دو فراتر از ±2SD.
اقدام: تحلیل دقیق روند و جستجوی Shift/Drift.
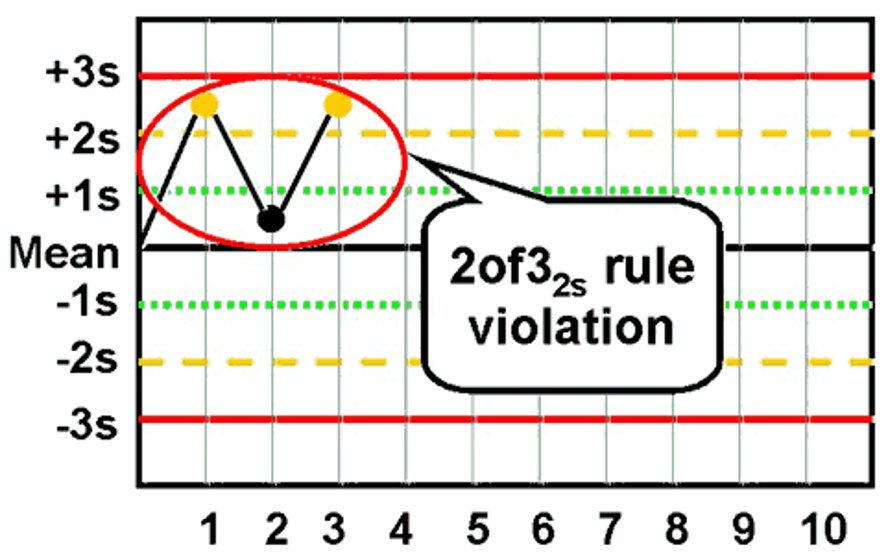
الگوی نموداری واقعی
| روز | مقدار کنترل | وضعیت |
|---|---|---|
| 1 | 100.5 | ✅ در محدوده |
| 2 | 101 | ✅ |
| 3 | 103 | ⚠️ +1SD |
| 4 | 104.5 | ❗ 1 2s |
| 5 | 105 | ❌ 2 2s |
الگوریتم تصمیمگیری روزانه IQC
- کنترلها را پیش از نمونههای بیمار اجرا کن.
- نتایج را با محدودههای پذیرش مقایسه کن.
- بر اساس قوانین Westgard تحلیل کن.
- در صورت خطا، گزارش بیمار را متوقف کن.
- اقدامات اصلاحی را انجام بده و مستند کن.
| قانون وستگارد | توصیف قانون | نوع خطا | اقدام بعدی |
|---|---|---|---|
| 1 2s | یک کنترل بیش از ۲ انحراف معیار از میانگین باشد. هشدار است، نه رد. | — | بهعنوان هشدار در نظر بگیر، اگر قوانین دیگر فعال شوند، بررسی کن. |
| 1 3s | یک نتیجه کنترل بیش از ±۳ SD از میانگین باشد. | تصادفی | رد سری آزمایش؛ تکرار کنترلها، بررسی پیپت، محلولها و تجهیزات. |
| 2 2s | دو نتیجه متوالی بیش از ۲ SD در یک سمت از میانگین. | سیستماتیک | رد سری؛ بررسی کالیبراسیون، واکنشگرها و خطاهای روش. |
| R 4s | تفاوت بین دو کنترل متوالی بیش از ۴ SD باشد (یکی بالا، یکی پایین). | تصادفی | رد سری؛ بررسی خطاهای نمونهگیری یا وسایل انتقال. |
| 4 1s | چهار نتیجه متوالی بیش از ۱ SD در یک سمت از میانگین. | سیستماتیک | رد سری؛ بررسی کالیبراسیون، تغییر تدریجی دما یا واکنشگر. |
| 10 x | ده نتیجه متوالی در یک سمت از میانگین (همه بالاتر یا پایینتر). | سیستماتیک | رد سری؛ نشانهٔ Bias پایدار است؛ کنترل و کالیبراسیون را بررسی کن. |
| 7 T | هفت نتیجه متوالی روند افزایشی یا کاهشی نشان دهند (Trend). | سیستماتیک (رانش تدریجی) | رد سری؛ بررسی عملکرد دستگاه و پایداری واکنشگرها. |
| 8 x | هشت نتیجه متوالی در یک سمت از میانگین (قانون سختتر از 10 x). | سیستماتیک | رد سری؛ بازبینی Bias و وضعیت کنترلها، تنظیم مجدد دستگاه. |
| 9 x | نه نتیجه متوالی در یک سمت میانگین (در برخی دستورالعملها جایگزین 10x). | سیستماتیک | بررسی Bias و احتمال تغییر در کالیبراسیون. |
| 12 x | دوازده کنترل متوالی در یک سمت میانگین؛ برای سیستمهای با تکرار زیاد. | سیستماتیک | بررسی کامل Bias و تعویض واکنشگر یا کالیبراسیون. |
کنترل کیفی خارجی (EQA / PT) و تحلیل دادهها
مقدمه
IQC پایداری داخلآزمایشگاهی را نشان میدهد، اما ممکن است با مقدار مرجع یا میانگین بینآزمایشگاهی اختلاف داشته باشید. EQA/PT برای سنجش صحت مطلق و مقایسه با دیگر آزمایشگاهها طراحی شده است.
۱) تعریف و اهداف
نهاد مرجع (وزارت بهداشت یا برنامههای بینالمللی مانند RIQAS، CAP، BIORAD EQAS) نمونههایی با غلظت معلوم ارسال میکند و نتایج شما با مقدار مرجع یا میانگین گروهی مقایسه میشود. اهداف: ارزیابی Accuracy، تشخیص Bias پایدار، مقایسه عملکرد، کشف خطاهای بلندمدت و مستندسازی برای ممیزیها.
۲) مراحل اجرا
دریافت نمونه مرجع → انجام آزمون دقیقاً مانند روند بیماران → ثبت و ارسال نتایج → دریافت گزارش تحلیلی.
۳) تفسیر Z-score
Z = (Your Result − Group Mean) / Group SD
بازه ۰ تا ±۲: قابل قبول ✅ | ±۲ تا ±۳: هشدار ⚠️ | بیش از ±۳: مردود ❌
| Z-score | تفسیر | وضعیت |
|---|---|---|
| ۰ تا ±۲ | عملکرد مناسب | قابل قبول ✅ |
| ±۲ تا ±۳ | نیازمند توجه | هشدار ⚠️ |
| > ±۳ | انحراف جدی | مردود ❌ |
نمونه عددی: کراتینین گروهی 1.0 mg/dL، SD=0.1، نتیجه شما 1.3 → Z=+3.0 → مردود → کالیبراسیون/معرف بررسی شود.
۴) نمونه گزارش تحلیلی
| پارامتر | Assigned Value | Your Result | SD | Z-score | تفسیر |
|---|---|---|---|---|---|
| Glucose | 98 | 99 | 1.5 | +0.66 | قابل قبول |
| Urea | 34 | 37 | 1.5 | +2.0 | هشدار |
| Creatinine | 1.0 | 1.3 | 0.1 | +3.0 | مردود |
۵) پیوند IQC و EQA
EQA وجود انحراف را آشکار میکند، اما برای یافتن علت به دادههای IQC نیاز دارید. پایش همزمان این دو، تصویر کاملتری از کیفیت ارائه میدهد.
۶) تحلیل آماری دادههای QC
۶.۱ میانگین و SD ماهانه
مقادیر ماهانه Mean/SD/CV را محاسبه و تغییرات را دنبال کنید.
نمونه: CV گلوکز مهر=2.0% و آبان=4.5% → هشدار (احتمال خرابی لامپ/معرف).
۶.۲ الگوهای Drift و Shift
| الگو | توضیح | علتهای محتمل |
|---|---|---|
| Shift | جابجایی ناگهانی به بالا/پایین | معرف یا کالیبراسیون جدید |
| Drift | تغییر تدریجی یکسویه | تبخیر معرف، تغییر حساسیت اپتیک |
| Random Scatter | پراکنده و بیقاعده | خطای اپراتور، حباب، خرابی پمپ |
نمونه: افزایش Mean ALT از 45 به 51 طی دو هفته → Drift مثبت → احتمال آلودگی معرف/افزایش دمای واکنش.
۷) اقدامات اصلاحی (CAPA)
روند پیشنهادی: تأیید خطا (تکرار با همان کنترل و کنترل تازه) → بررسی علل (معرف/کنترل/کالیبراسیون/کووت/حجم/دما) → اجرای اقدام (تعویض معرف، کالیبراسیون، تمیزکاری، تنظیم دما) → ثبت و اطلاع → تأیید با اجرای مجدد کنترلها.
فرمها، چکلیستها و جمعبندی آموزشی در مورد کنترل کیفی بیوشیمی
۱) مستندسازی در کنترل کیفی بیوشیمی
بدون ثبت منظم، حتی اجرای عالی QC در ممیزی فاقد پشتوانه تلقی میشود. سه سطح ثبت توصیه میشود:
- لاگ روزانه (IQC Log): کنترلها، محدودهها، وضعیت قبول/رد.
- تحلیل ماهانه: Mean/SD/CV، نمودارهای Levey–Jennings و روندها.
- CAPA: خطاها، علل ریشهای، اقدامات اصلاحی/پیشگیرانه و نتیجه.
۲) نمونه فرم ثبت روزانه کنترل کیفی بیوشیمی
| تاریخ | تست | سطح کنترل | نتیجه | محدوده مجاز | قانون فعال | وضعیت | اقدام اصلاحی | اپراتور | تأیید QC |
|---|---|---|---|---|---|---|---|---|---|
| 1404/08/12 | Glucose | Normal | 104.2 | 97–103 | 1 2s | هشدار | تکرار کنترل | احمدی | ✔️ |
| 1404/08/13 | Glucose | Normal | 105.1 | 97–103 | 2 2s | مردود | تعویض معرف، کالیبراسیون | احمدی | ✔️ |
| 1404/08/13 | ALT | Patho | 52 | 42–48 | 1 3s | مردود | کنترل دمای انکوباتور | احمدی | ✔️ |
۳) فرم تحلیل ماهانه کنترل کیفی بیوشیمی
| تست | Mean | SD | CV% | تغییر نسبت به ماه قبل | نتیجه تحلیل | اقدام |
|---|---|---|---|---|---|---|
| Glucose | 100 | 1.5 | 1.5 | ثابت | عالی | ادامه |
| Urea | 33 | 2.0 | 6.0 | +2% | ناپایداری رو به افزایش | بررسی پمپ معرف |
| Creatinine | 1.00 | 0.05 | 5.0 | ثابت | قابل قبول | — |
| ALT | 45 | 3.0 | 6.6 | +1.6% | افزایش جزئی | پایش دمای انکوباتور |
۴) فرم CAPA (اقدامات اصلاحی/پیشگیرانه) در کنترل کیفی بیوشیمی
| تاریخ | تست | نوع خطا | قانون | علت احتمالی | اقدام اصلاحی | نتیجه پس از اصلاح | تأیید QC |
|---|---|---|---|---|---|---|---|
| 1404/08/10 | ALT | سیستماتیک | 10x | Drift مثبت | کالیبراسیون + تعویض معرف | OK | ✔️ |
| 1404/08/18 | Na⁺ | تصادفی | R4s | پیپتینگ نادرست | سرویس پیپت + آموزش | OK | ✔️ |
۵) فرم لاگ بوک کنترل کیفی بیوشیمی
| تاریخ دریافت | برنامه | تست | مقدار مرجع | نتیجه شما | Z-score | تفسیر | اقدام اصلاحی |
|---|---|---|---|---|---|---|---|
| 1404/06/20 | RIQAS | Glucose | 100 | 99 | -0.5 | قابل قبول | — |
| 1404/06/20 | RIQAS | Creatinine | 1.0 | 1.3 | +3.0 | مردود | کالیبراسیون مجدد |
۶) چکلیستهای روزانه و ماهانه کنترل کیفی بیوشیمی
- دمای انکوباتور (37±0.5°C) هر شیفت بررسی شود.
- کووتها و مسیر نوری تمیز باشد؛ پایداری نور اطمینانیابی شود.
- تاریخ انقضای معرفها و کنترلها کنترل شود.
- حداقل دو سطح کنترل (نرمال و پاتولوژیک) در هر سری اجرا گردد.
- نتایج در لاگ IQC ثبت و با Levey–Jennings تحلیل شود.
- برای تستهای حیاتی از سه سطح کنترل بهره ببرید (Low/Normal/High).
- هر ۶ ماه محدودههای Mean و SD بازنگری شود.
سؤالات متداول (FAQ) در مورد کنترل کیفی بیوشیمی
۱) کنترل کیفی بیوشیمی چیست؟
فرآیندی نظاممند برای تضمین صحت، دقت و تکرارپذیری نتایج آزمونهای بیوشیمی در محیط آزمایشگاه.
۲) تفاوت IQC و EQA چیست؟
IQC پایداری روزانه سیستم را پایش میکند؛ EQA صحت مطلق را در مقایسه با مقدار مرجع یا میانگین گروهی میسنجد.
۳) چرا قوانین Westgard اهمیت دارند؟
چون با تحلیل آماری نقاط کنترل، وقوع خطاهای تصادفی و سیستماتیک پیش از اثرگذاری بر گزارش بیماران مشخص میشود.
۴) محدودهی مجاز کنترل چگونه تعیین میشود؟
با حداقل ۲۰ اندازهگیری اولیه برای هر سطح کنترل و محاسبهی Mean ± 2SD.
۵) اگر 1 3s فعال شود چه میشود؟
خروج از ±3SD به معنی مردودی فوری سری است؛ باید کنترل تکرار و معرف/کالیبراسیون/دمای انکوباتور بررسی شود.
۶) قانون R 4s چه خطایی را نشان میدهد؟
خطای تصادفی (پیپتینگ، حباب، نوسان دما)؛ باید هر دو کنترل تکرار و ابزار بررسی شوند.
۷) Drift و Shift چگونه تشخیص داده میشود؟
Shift جابجایی ناگهانی نتایج است (معرف یا کالیبراسیون جدید) و Drift تغییر تدریجی در یک جهت (مثلاً تبخیر معرف).
۸) CV% قابل قبول برای تستها؟
گلوکز <3%، آنزیمها <6%، الکترولیتها <2%، پروتئینها <5%.
۹) در ممیزی QC چه چیزهایی بررسی میشود؟
نمودارهای Levey–Jennings، لاگهای روزانه IQC، تحلیلهای ماهانه (CV/SD)، فرمهای CAPA و نتایج EQA.
۱۰) چه زمانی باید Mean و SD بازنگری شوند؟
دستکم هر ۶ ماه یکبار یا پس از تعویض سری معرف/کنترل و بعد از سرویس اساسی دستگاه.
