تیتراسیون چیست؟ آموزش کامل تیتراسیون برای دانشجویان شیمی و علوم آزمایشگاهی
تیتراسیون چیست؟ تیتراسیون یک روش تجزیه حجمی در شیمی است که برای تعیین غلظت دقیق یک ماده در محلول، با استفاده از محلول استاندارد (تیترانت) و اندازهگیری حجم مصرفشده بهکار میرود. این تکنیک در آزمایشگاههای شیمی، علوم آزمایشگاهی، داروسازی، صنایع غذایی و محیطزیست برای کنترل کیفیت و آنالیز کمی مواد استفاده میشود.
در این راهنمای جامع، ابتدا به تعریف و مفهوم تیتراسیون، سپس به اصول چهارگانهی آن، و در ادامه به انواع مهم تیتراسیون (اسید–باز، کمپلکسومتری، رسوبی، ردوکس، برگشتی و ابزارمحور) پرداخته میشود تا دیدی کامل و کاربردی به دانشجویان شیمی و علوم آزمایشگاهی بدهد.
جهت عضویت در کانال آموزشی در تلگرام به لینک زیر مراجعه کنید:
https://t.me/hematology_education
فهرست مطالب تیتراسیون چیست
مقدمه: تیتراسیون چیست و چه نقشی در شیمی تجزیه دارد؟
در این بخش، به صورت پایهای و آموزشی توضیح میدهیم تیتراسیون چیست، چرا در شیمی تجزیه و در آزمایشگاههای علوم آزمایشگاهی اینقدر مهم است و چه جایگاهی در آنالیز کمی دارد.
تیتراسیون یکی از بنیادیترین روشهای تجزیهٔ کمی در شیمی تجزیه است که بر پایهٔ اندازهگیری حجم محلول استاندارد برای تعیین غلظت یک آنالیت انجام میگیرد. اهمیت تیتراسیون از این واقعیت ناشی میشود که بسیاری از سنجشهای آزمایشگاهی—از کنترل کیفیت نمونههای دارویی و غذایی تا آنالیزهای محیطی و صنعتی—نیازمند تعیین غلظت دقیق یک ترکیب هستند و تیتراسیون یکی از قابلاعتمادترین روشهای رسیدن به این هدف است.
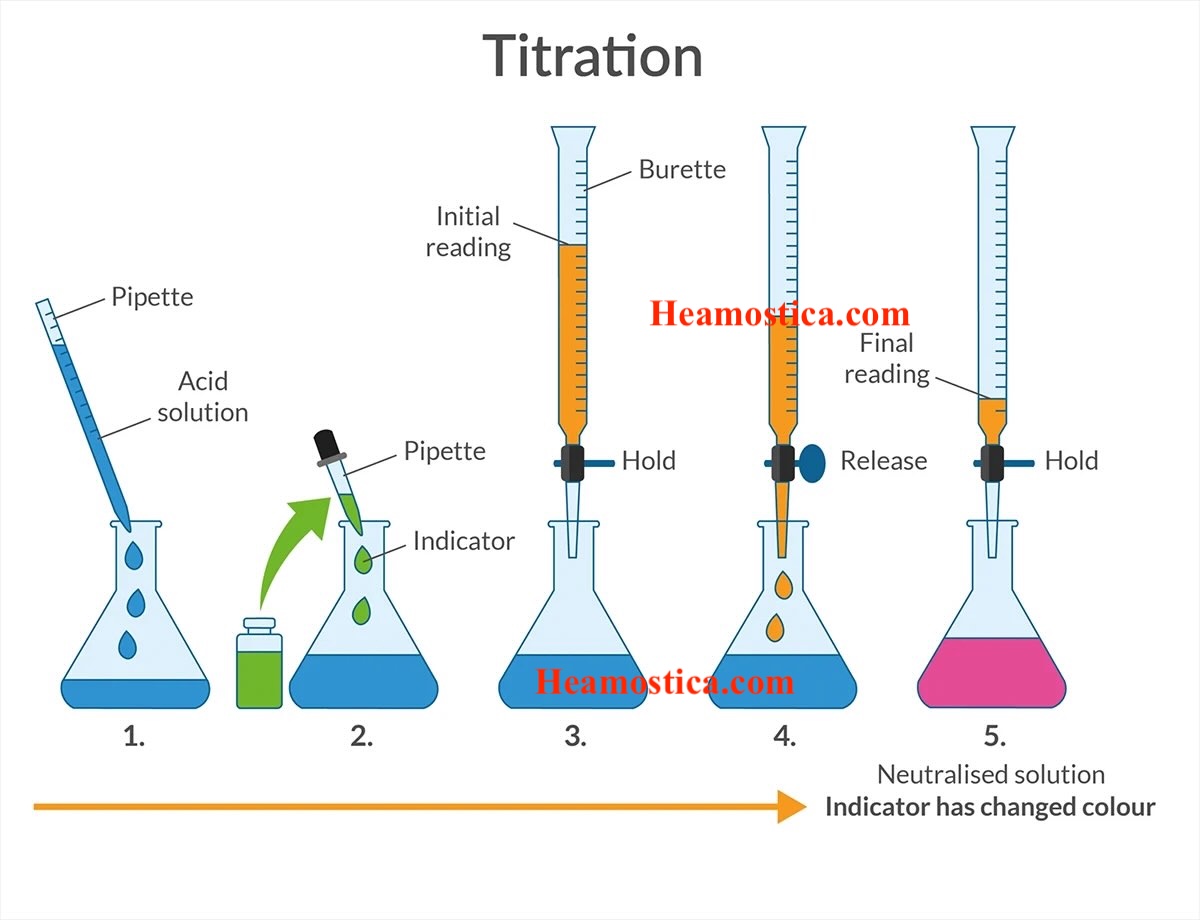
در یک فرایند تیتراسیون، معمولاً آنالیت (مادهٔ مجهول) در یک ارلن یا بشر قرار میگیرد و تیترانت (محلول استاندارد با غلظت معلوم) از طریق بورت بهتدریج به آن اضافه میشود. با پیشرفت واکنش، تغییرات شیمیایی مشخصی رخ میدهد که رسیدن به «نقطهٔ پایان» را مشخص میکند. این تغییر معمولاً با یک اندیکاتور شیمیایی (تغییر رنگ)، یا با استفاده از روشهای ابزاری مانند pH متر، پتانسیومتر یا هدایتسنج تشخیص داده میشود.
تیتراسیون به دلیل برخورداری از چند مزیت مهم—از جمله دقت بالا، سادگی، هزینهٔ کم، قابلیت اجرای سریع و نیاز حداقلی به تجهیزات پیچیده—به یکی از اولین و مهمترین مهارتهای عملی در آزمایشگاههای شیمی و علوم آزمایشگاهی تبدیل شده است.
درک صحیح از اینکه «تیتراسیون چیست» و چه محدودیتهایی دارد، برای جلوگیری از تفسیر اشتباه نتایج آزمایشگاهی ضروری است؛ تیتراسیون فقط یک عمل حجمی نیست، بلکه یک روش دقیق استوکیومتری است.
کاربردهای مهم تیتراسیون در آزمایشگاه: تیتراسیون چیست در عمل؟
برای درک بهتر مفهوم تیتراسیون چیست، باید بدانیم این روش دقیقاً در چه سناریوهایی در آزمایشگاههای شیمی و علوم آزمایشگاهی بهکار میرود.
کاربردهای مهم تیتراسیون
- تعیین غلظت اسیدها و بازها در صنایع غذایی، دارویی و پتروشیمی
- سنجش سختی آب بر اساس مقدار یونهای Ca²⁺ و Mg²⁺
- اندازهگیری کلر، ید، پرمنگنات، دیکرومات و سایر اکسندهها و کاهندهها
- تعیین مقدار فلزات سنگین در نمونههای محیطی
- تعیین درصد خلوص مواد شیمیایی خشک
- سنجش ترکیبات آلی دارای گروههای فعال (آمینها، فنولها، اسیدهای آلی)
- کاربردهای وسیع در بیوشیمی (پروتئینها، آمینواسیدها، آلکالوئیدها)
هنگام طراحی یک روش تیتراسیون در آزمایشگاه، باید نوع نمونه، محدوده غلظت، تداخلها و نیاز به دقت/سرعت را همزمان در نظر بگیرید؛ انتخاب اشتباه نوع تیتراسیون میتواند به نتایج کاملاً غلط منجر شود.
اصول چهارگانهٔ تیتراسیون چیست؟ (گسترده و تحلیلی)
برای پاسخ کامل به سؤال تیتراسیون چیست، فقط تعریف کافی نیست؛ باید اصول پایهای طراحی و اجرای یک تیتراسیون قابلاعتماد را بشناسیم. این بخش، چهار اصل حیاتی در تیتراسیون را بهصورت تحلیلی بررسی میکند.
۱. واکنش باید کامل، سریع و با استوکیومتری دقیق باشد
برای اینکه تیتراسیون معتبر باشد، واکنش میان تیترانت و آنالیت باید:
- بهطور کامل انجام شود: یعنی پس از افزودن مقدار کافی تیترانت، هیچ مقداری از آنالیت واکنشنداده باقی نماند.
- دارای نسبت مولی مشخص باشد: مثلاً در تیتراسیون اسید–باز، نسبت خنثیسازی ۱:۱ است، اما در تیتراسیون پرمنگنات با آهن(II)، نسبت 1:5 است.
- به اندازه کافی سریع باشد: واکنشهای کند یا چندمرحلهای در تیتراسیون قابل استفاده نیستند، چون نقطه پایان مبهم میشود.
این اصل اساس تمام محاسبات تیتراسیون است؛ اگر واکنش ناقص یا برگشتپذیر باشد، نتیجه بهطور قطع اشتباه خواهد بود.
۲. استفاده از محلول استاندارد پایدار و دقیق (Titrant)
تیترانت قلب تیتراسیون است. یک تیترانت معتبر باید:
- غلظت معلوم و دقیق داشته باشد (Normality یا Molarity مشخص و ثابت)
- در زمان، هوا، نور یا واکنشهای جانبی دچار تغییر نشود
- بتوان آن را با یک استاندارد اولیه (Primary Standard) دقیق تنظیم کرد
نمونههای کلیدی استاندارد اولیه:
- KHP (فتالات اسید پتاسیم) برای استاندارد کردن NaOH
- آرسنیک تریاکسید برای استاندارد کردن یدومتری
- Na₂CO₃ خشک برای استاندارد کردن اسیدها
اگر تیترانت پایدار نباشد، کل تیتراسیون بیاعتبار میشود. بهعنوان مثال، NaOH بهشدت CO₂ هوا را جذب میکند، بنابراین بدون استانداردسازی دقیق نمیتوان از آن استفاده کرد.
۳. امکان تشخیص واضح نقطهٔ پایان
نقطهٔ پایان باید واضح، تکرارپذیر و نزدیک به نقطهٔ معادل باشد.
روشهای تشخیص نقطه پایان:
- اندیکاتورهای رنگی (فنلفتالئین، متیل اورنج، ایندوفنول)
- اندازهگیری pH در اسید–باز
- پتانسیومتری در اکسایش–کاهش
- هدایتسنجی برای نمکهای قوی و محلولهای بیرنگ
- اسپکتروفتومتری برای نمونههایی که رنگ طبیعی دارند
خطا زمانی ایجاد میشود که نقطه پایان خیلی زود یا دیر تشخیص داده شود، که اصطلاحاً «خطای اندیکاتور» نامیده میشود.
۴. اندازهگیری دقیق حجم و اجرای صحیح تکنیک آزمایشگاهی
زیرساخت یک تیتراسیون دقیق، تکنیک صحیح اندازهگیری حجم است:
- بورت باید تمیز، کالیبره و بدون حباب باشد
- منیسک باید در سطح چشم خوانده شود
- دما باید کنترل شود، چون دما روی حجم اثر میگذارد
- باید از اسپلاشرها و شستوشوی دیوارههای ارلن استفاده شود
- ریختن تیترانت باید یکنواخت باشد، نه سریع و ناگهانی
کوچکترین خطای حجمی میتواند کل نتیجه را دچار خطای جدی کند.
اگر در عمل متوجه شدید که «تیتراسیون چیست» را میدانید ولی نتایج شما تکرارپذیر نیست، تقریباً همیشه مشکل در یکی از همین چهار اصل است: واکنش، تیترانت، نقطه پایان یا تکنیک حجمی.
انواع تیتراسیون چیست؟ (با توضیحات گسترده و مثالهای کاربردی)
برای تکمیل پاسخ به سؤال تیتراسیون چیست، باید با انواع مختلف این روش آشنا شوید؛ زیرا هر نوع تیتراسیون برای گروه خاصی از نمونهها و آنالیتها مناسب است.
۱. تیتراسیون اسید–باز
این شناختهشدهترین و پرکاربردترین نوع تیتراسیون است.
بر اساس واکنش خنثیسازی و تغییرات pH انجام میشود. جهت مطالعه ی جامع در مورد تیتراسیون اسید باز به لینک زیر مراجعه کنید :
تیتراسیون اسید باز چیست؟ آموزش کامل تیتراسیون اسید–باز برای دانشجویان شیمی و علوم آزمایشگاهی
نمونهها:
- Titration of HCl with NaOH
- Titration of acetic acid with KOH
- Determination of alkalinity/acidity of water
اندیکاتور مهم: فنلفتالئین (pH ~ 8.2–10)، متیل اورنج (pH ~ 3.1–4.4)
اهمیت آموزشی: این نوع، پایهٔ درک منحنی تیتراسیون و نقطه معادل است.
برای آشنایی عملیتر با اندیکاتور فنلفتالئین در تیتراسیون اسید–باز، میتوانید مقالهٔ زیر را مطالعه کنید:
روش تهیه محلول فنل فتالئین: راهنمای آموزشی برای کارشناسان
۲. تیتراسیون کمپلکسومتری (Complexometric)
این نوع بر اساس تشکیل کمپلکس پایدار میان یون فلزی و عامل کمپلکسدهنده انجام میشود.
EDTA مهمترین تیترانت این روش است.
کاربرد اصلی:
- سنجش سختی آب (Ca²⁺ و Mg²⁺)
- اندازهگیری Cu²⁺ ،Zn²⁺ ،Pb²⁺ ،Fe³⁺ و سایر فلزات
اندیکاتورهای رایج:
- اریوکروم بلک T
- مورکسید
این تیتراسیون یکی از مهمترین روشها در صنایع آب، معدن و محیطزیست است.
۳. تیتراسیون رسوبی (Precipitation)
مبنای این روش تشکیل رسوب نامحلول است.
معروفترین مثال:
- تیتراسیون یون کلرید با نیترات نقره (روش Mohr)
روشها:
- Mohr (اندیکاتور کرومات)
- Volhard (پشتتیتراسیون با تیوسیانات)
- Fajans (اندیکاتور جذب سطحی)
کاربرد:
- اندازهگیری کلر و برم در آب و محصولات غذایی
- سنجش هالوژنیدها در ترکیبات معدنی و آلی
۴. تیتراسیون اکسایش–کاهش (Redox)
این روش بر مبنای انتقال الکترون است.
نمونهها:
- تیتراسیون آهن(II) با پرمنگنات (MnO₄⁻)
- تیتراسیون یدیمتر/یدومتری (I₂ / S₂O₃²⁻)
- تیتراسیون دیکرومات با آهن(II)
مزیت: اغلب نیازی به اندیکاتور ندارد (مثلاً MnO₄⁻ خودش رنگزا است).
کاربرد:
- تجزیه فلزات
- سنجش اکسیژن محلول
- کنترل کیفیت فرآیندهای صنعتی
۵. تیتراسیون برگشتی (Back Titration)
زمانی استفاده میشود که واکنش مستقیم کند یا نامناسب باشد.
مثال:
- تعیین مقدار کربنات کلسیم در سنگ آهک
- تعیین آمینهای آلی
- آنالیز فلزات با واکنشهای آهسته
فرایند:
- افزودن مقدار دقیقی از تیترانت اضافی
- واکنش تیترانت با آنالیت
- تیتراسیون مقدار اضافی با محلول دوم
۶. تیتراسیون ابزارمحور (Instrumental Titration)
برای نمونههای رنگی، کدر یا پیچیده.
ابزارها:
- pH متر → اسید–باز
- پتانسیومتر → ردوکس
- هدایتسنج → محلولهای یونی
- اسپکتروفتومتر → تغییرات جذب نوری
مزیت:
- دقت بسیار بالا
- مناسب برای محیطهای پیچیده که اندیکاتور جواب نمیدهد
قبل از شروع آزمایش، فقط نپرسید «تیتراسیون چیست»، بلکه بپرسید «کدام نوع تیتراسیون برای این نمونه و این محدوده غلظت مناسبتر است؟» انتخاب درست نوع تیتراسیون، تفاوت بین یک نتیجه قابلاستناد و یک عدد بدون ارزش تحلیلی است.
سوالات متداول درباره تیتراسیون چیست (FAQ)
۱. تیتراسیون چیست و در یک جمله چگونه تعریف میشود؟
تیتراسیون روشی در شیمی تجزیه است که در آن با افزودن تدریجی یک محلول استاندارد (تیترانت) به نمونه مجهول و اندازهگیری حجم مصرفی، غلظت آنالیت با استفاده از روابط استوکیومتری محاسبه میشود.
۲. تفاوت نقطه معادل و نقطه پایان در تیتراسیون چیست؟
نقطه معادل (Equivalence Point) لحظهای است که مقدار تیترانت از نظر استوکیومتری دقیقاً با مقدار آنالیت برابر میشود؛ اما نقطه پایان (End Point) لحظهای است که ما به کمک اندیکاتور یا دستگاه آن را مشاهده میکنیم. هر چه فاصله این دو کمتر باشد، دقت تیتراسیون بیشتر است.
۳. چرا انتخاب اندیکاتور مناسب در تیتراسیون اسید–باز مهم است؟
هر اندیکاتور در یک بازه pH خاص تغییر رنگ میدهد. اگر بازه تغییر رنگ اندیکاتور با ناحیه جهش pH در نقطه معادل منطبق نباشد، نقطه پایان زودتر یا دیرتر دیده میشود و نتیجه دچار خطای قابلتوجه خواهد شد.
۴. مهمترین خطاهای رایج در تیتراسیون چیست؟
مهمترین خطاها شامل: خواندن غلط منیسک، وجود حباب در بورت، عدم شستوشوی دیواره ارلن با تیترانت، استفاده از تیترانت ناپایدار، انتخاب اندیکاتور نامناسب و عجله در نزدیک نقطه پایان است.
۵. چرا تیتراسیون هنوز در کنار روشهای دستگاهی مدرن استفاده میشود؟
بهدلیل سادگی، هزینه کم، قابلیت اجرا در اکثر آزمایشگاهها، دقت قابل قبول و عدم نیاز به تجهیزات پیچیده، تیتراسیون همچنان یکی از ستونهای اصلی آنالیز کمی در شیمی و علوم آزمایشگاهی است.
۶. برای اجرای یک تیتراسیون دقیق، چه پیشنیازهایی لازم است؟
نیاز به شیشهآلات کالیبره (بورت، پیپت، بالن ژوژه)، تیترانت استاندارد و پایدار، اندیکاتور مناسب، کنترل دما، رعایت اصول کار با بورت و آشنایی با استوکیومتری واکنش دارید.
۷. در تیتراسیون اسید–باز، چرا اغلب از فنلفتالئین استفاده میشود؟
فنلفتالئین برای تیتراسیون اسید قوی–باز قوی و اسید ضعیف–باز قوی مناسب است، چون بازه تغییر رنگ آن (حدود ۸٫۲ تا ۱۰) با جهش pH نزدیک نقطه معادل این سیستمها همخوانی دارد و تغییر رنگ آن واضح و تکرارپذیر است.
۸. در تیتراسیون کمپلکسومتری با EDTA چه نکتهای بسیار مهم است؟
pH محیط نقش حیاتی دارد، چون پایداری کمپلکسهای فلزی–EDTA بهشدت به pH وابسته است. بنابراین استفاده از بافر مناسب و اندیکاتور اختصاصی فلز مورد نظر ضروری است.
۹. چه زمانی از تیتراسیون برگشتی استفاده میکنیم؟
زمانی که واکنش مستقیم میان تیترانت و آنالیت بسیار کند، ناقص یا از نظر عملیاتی دشوار است، مقدار اضافی از تیترانت را به نمونه اضافه کرده و سپس تیترانت اضافی را با محلول استاندارد دیگری تیتراسیون میکنیم.
۱۰. نقش تیتراسیون در علوم آزمایشگاهی پزشکی چیست؟
در علوم آزمایشگاهی پزشکی، تیتراسیون در تعیین سختی آب، آمادهسازی محلولهای بافر، استانداردسازی محلولها، برخی سنجشهای سرولوژی و تنظیم دقیق pH محیطهای کشت و کیتها بهکار میرود و در کنترل کیفیت روشها نقش مهمی دارد.
منابع معتبر برای مطالعه بیشتر درباره تیتراسیون چیست
