کنترل کیفی آزمایشگاه تشخیص پزشکی
کنترل کیفی آزمایشگاه تشخیص طبی شامل مجموعهای از اقدامات سیستماتیک برای پایش دقت و صحت نتایج آزمایشها، اعتبارسنجی روشها، اجرای کنترل کیفی داخلی و تحلیل دادهها با استفاده از نمودار لویجنینگ و قوانین وستگارد است. هدف نهایی کنترل کیفیت در آزمایشگاه تشخیصی، ارائه نتایج قابلاعتماد به پزشک و بیمار و حفظ استانداردهای بینالمللی در سیستم مدیریت کیفیت آزمایشگاه است.
جهت عضویت در کانال آموزشی در تلگرام به لینک زیر مراجعه کنید:
https://t.me/hematology_education
فهرست مطالب کنترل کیفی آزمایشگاه
مقدمه
مفاهیم پایه تضمین کیفیت و سیستم مدیریت کیفیت در آزمایشگاه
مفهوم صحت، دقت، Trueness و Bias
اعتبارسنجی (Validation) روشها
کنترل کیفی داخلی (IQC) در آزمایشگاه تشخیص پزشکی
رسم نمودار لویجنینگ در اکسل
قوانین وستگارد در کنترل کیفیت نتایج آزمایشگاهی
تحلیل خطاها و اقدامات اصلاحی
کنترل کیفی خارجی (EQA/PT) در آزمایشگاه تشخیصی
مستندسازی، بازنگری و جمعبندی کنترل کیفیت در آزمایشگاه
سوالات متداول
منابع معتبر برای مطالعه بیشتر
مقدمه
کنترل کیفی (Quality Control – QC) یکی از بنیادیترین ارکان تضمین کیفیت (Quality Assurance – QA) در آزمایشگاههای تشخیص پزشکی است.
هدف از کنترل کیفی، اطمینان از صحت (Accuracy) و دقت (Precision) نتایج آزمایشها و در نهایت افزایش اعتماد پزشک و بیمار به گزارشهای آزمایشگاه است.
نتیجهی هر آزمایش، تنها زمانی ارزش بالینی دارد که بهدرستی، دقت و تکرارپذیری آن اطمینان حاصل شود. این هدف از طریق استقرار یک سیستم مدیریت کیفیت (Quality Management System – QMS) در تمامی مراحل پیشتحلیلی، تحلیلی و پستحلیلی محقق میشود. در واقع، کنترل کیفی آزمایشگاه بخشی جداییناپذیر از کیفیت کلی خدمات تشخیصی است.
نکته مهم در کنترل کیفی آزمایشگاه:
بدون استقرار کنترل کیفی مؤثر، حتی پیشرفتهترین تجهیزات نیز نمیتوانند تضمینکننده صحت نتایج باشند. فرهنگ کیفیت باید در تمام سطوح آزمایشگاه نهادینه شود.
به منظور مطالعه ی جامع در مورد کنترل کیفی در بخش های مختلف آزمایشگاه به لینک های زیر مراجعه کنید:
رسم نمودارد لوی جنین در اکسل
بخش ۱: مفاهیم پایه در تضمین کیفیت و سیستم مدیریت کیفیت در آزمایشگاه
درک مفاهیم تضمین کیفیت و مدیریت کیفیت برای پیادهسازی صحیح کنترل کیفی آزمایشگاه تشخیص پزشکی ضروری است. این مفاهیم چارچوب نظری و عملی برای پایش و بهبود کیفیت نتایج را فراهم میکنند.
۱.۱ تضمین کیفیت (Quality Assurance – QA)
تضمین کیفیت مجموعهای از اقدامات سیستماتیک و برنامهریزیشده است که برای اطمینان از صحت فرآیندهای کاری در آزمایشگاه انجام میشود.
QA چتری است که همهی اجزای سیستم کیفیت از جمله کنترل کیفی داخلی (IQC)، کنترل کیفی خارجی (EQA)، کالیبراسیون، آموزش پرسنل، نگهداری تجهیزات، و مستندسازی را دربرمیگیرد.
نمونهای از اقدامات QA در آزمایشگاه:
– تعیین مسئول کنترل کیفیت در هر بخش
– تهیهی دستورالعملهای استاندارد کاری (SOPs)
– ثبت و آرشیو مستندات کنترل کیفی
– آموزش و ارزیابی صلاحیت پرسنل
– پایش دمای یخچالها و انکوباتورها
۱.۲ سیستم مدیریت کیفیت (Quality Management System – QMS) در آزمایشگاه تشخیصی
سیستم مدیریت کیفیت بر اساس استاندارد بینالمللی ISO 15189 طراحی میشود.
QMS تمام فعالیتهای آزمایشگاه را از پذیرش نمونه تا گزارش نهایی در یک چارچوب منسجم هدایت میکند و نقش بسیار مهمی در عملکرد صحیح کنترل کیفی آزمایشگاه دارد.
اجزای اصلی QMS عبارتاند از:
1. مدیریت سازمانی و مسئولیتها
2. مدیریت منابع انسانی و تجهیزات
3. کنترل مدارک و سوابق
4. ارزیابی کیفیت خدمات
5. بهبود مستمر (Continuous Improvement)
هدف نهایی QMS، ایجاد یک چرخهی بهبود دائمی است که خطاها را شناسایی، اصلاح و پیشگیری کند و به این ترتیب، کنترل کیفیت در آزمایشگاه بهصورت مستمر و نظاممند اجرا شود.
۱.۳ مدیریت کیفیت جامع (Total Quality Management – TQM)
در TQM همهی افراد، از مدیر فنی گرفته تا اپراتور دستگاه، در بهبود کیفیت سهیم هستند.
ایدهی اصلی این رویکرد این است که کیفیت، یک بخش مجزا نیست بلکه در تمام فعالیتهای روزمره باید جاری باشد. در این چارچوب، کنترل کیفی آزمایشگاه تنها یک وظیفه اداری نیست، بلکه وظیفهای مشترک برای کل تیم آزمایشگاه است.
استقرار QA، QMS و TQM در کنار هم، زیرساخت لازم برای اجرای موفق کنترل کیفی آزمایشگاه تشخیص پزشکی را فراهم میکند و بدون این زیرساخت، حتی بهترین کنترلها هم به نتیجه مطلوب نمیرسند.
بخش ۲: مفاهیم Accuracy، Precision، Trueness و Bias در کنترل کیفیت آزمایشگاه
یکی از پایههای تئوریک کنترل کیفی آزمایشگاه، فهم تفاوت بین صحت، دقت و Bias است. این مفاهیم کمک میکنند تا بدانیم مشکل یک روش تحلیلی از نوع خطای تصادفی است یا سیستماتیک.
در کنترل کیفی، چهار واژهی مهم وجود دارد که باید دقیق درک شوند:
| مفهوم | تعریف | مثال |
|---|---|---|
| Accuracy (صحت) | نزدیکی میانگین نتایج به مقدار واقعی | مقدار واقعی سدیم 140 mmol/L؛ نتیجه میانگین 139.5 → صحت بالا |
| Precision (دقت) | تکرارپذیری نتایج در شرایط یکسان | پنج بار تکرار با نتایج نزدیک به هم نشاندهندهی دقت بالا |
| Trueness (درستی) | نشاندهندهی نبود خطای سیستماتیک | میانگین نتایج در نزدیکی مقدار مرجع قرار دارد |
| Bias (انحراف) | اختلاف میانگین نتایج و مقدار واقعی | مقدار واقعی 100، میانگین آزمایشگاه 104 → Bias = +4% |
تحلیل:
گاهی روش آزمایش دقیق است اما صحیح نیست (یعنی نتایج تکرارپذیر ولی منحرف از مقدار واقعی هستند). در این حالت، خطای سیستماتیک وجود دارد و نیاز به کالیبراسیون یا بررسی معرفها است. در کنترل کیفی آزمایشگاه، تشخیص این نوع خطاها برای اصلاح بهموقع روشها حیاتی است.
بخش ۳: اعتبارسنجی روشها (Validation) در کنترل کیفیت آزمایشگاه
اعتبارسنجی یعنی بررسی علمی عملکرد روش آزمایشگاهی برای اطمینان از اینکه روش مورد استفاده، برای هدف مورد نظر مناسب است.
در آزمایشگاههای تشخیص پزشکی، قبل از استفاده از هر روش جدید، لازم است پارامترهای اعتبارسنجی بررسی و مستند شوند تا کنترل کیفی بر پایهای محکم استوار باشد.
| پارامتر | توضیح | مثال |
|---|---|---|
| دقت (Precision) | بررسی تکرارپذیری روزانه و بینروزی | انجام 10 بار آزمایش روی کنترل نرمال و پاتولوژیک |
| صحت (Accuracy) | مقایسه با روش مرجع یا کنترل مرجع | مقایسه نتایج با مقادیر Reference Material |
| خطی بودن (Linearity) | بررسی صحت نتایج در غلظتهای مختلف | رقیقسازی نمونهها در 5 غلظت متفاوت |
| حد تشخیص (LOD) | پایینترین مقدار قابل شناسایی | مثلاً 0.1 mg/dL |
| پایداری (Stability) | بررسی پایداری نتایج در نگهداری طولانی | نگهداری کنترل در 4°C به مدت 7 روز و مقایسه نتایج |
هر روشی که بدون اعتبارسنجی وارد روتین آزمایشگاه شود، میتواند منجر به خطاهای پنهان و تهدیدی جدی برای کیفیت نتایج آزمایشگاهی و ایمنی بیمار باشد. اعتبارسنجی، نقطه شروع کنترل کیفی در آزمایشگاه است.
بخش ۴: کنترل کیفی داخلی (Internal Quality Control – IQC) در آزمایشگاه تشخیصی
کنترل کیفی داخلی بهمنظور پایش مستمر عملکرد دستگاه و روش انجام میشود. در این روش، از نمونههای کنترل با مقادیر شناختهشده استفاده میشود.
اجرای صحیح IQC یکی از ارکان اصلی کنترل کیفی در آزمایشگاه های تشخیص پزشکی است.
مراحل اجرای IQC در کنترل کیفی آزمایشگاه
1. انتخاب ماده کنترل:
– کنترل نرمال (Normal control)
– کنترل پاتولوژیک (Abnormal control)
2. تعیین میانگین و انحراف معیار:
پس از 20 اندازهگیری اولیه، میانگین (Mean) و انحراف معیار (SD) محاسبه میشود.
3. اندازهگیری روزانه کنترلها:
هر روز قبل از شروع کار یا در هر شیفت کاری، کنترلها بررسی میشوند.
4. ثبت دادهها و رسم نمودار لویجنینگ:
نتایج روی نمودار رسم شده و روندها بررسی میشوند.
5. تحلیل بر اساس قوانین وستگارد:
اگر نتیجه از محدوده مجاز خارج شد، باید علتیابی و اصلاح شود.
مثال عملی:
کنترل نرمال با مقدار هدف 100 و SD=2 در نظر بگیرید. نتایج روزانه طی 10 روز:
100، 99، 98، 101، 100، 103، 104، 105، 106، 107
در روز دهم مقدار 107 خارج از محدودهی 3SD است → کنترل رد شده است.
بخش ۵: رسم نمودار لویجنینگ (Levey-Jennings) در اکسل برای کنترل کیفی آزمایشگاه
نمودار لویجنینگ ابزاری است برای نمایش گرافیکی نتایج کنترل نسبت به میانگین و انحراف معیار. این نمودار به کارشناسان کمک میکند تا تغییرات کوچک و تدریجی در عملکرد سیستم را در قالب کنترل کیفی آزمایشگاه تشخیص دهند.
گامبهگام رسم نمودار لویجنینگ در Excel
1. وارد کردن دادهها:
– ستون A: شماره روزها (Day 1, Day 2, …)
– ستون B: نتایج کنترلها (مثلاً 98، 100، 101، 104…)
2. محاسبهی میانگین و SD:
– Mean: =AVERAGE(B2:B21)
– SD: =STDEV(B2:B21)
3. ایجاد ستونهای ±1SD، ±2SD، ±3SD:
– Mean + SD، Mean - SD و به همین ترتیب برای ±2SD و ±3SD
4. انتخاب دادهها و رسم نمودار:
– مسیر: Insert → Line Chart → Line with Markers
– خطوط Mean، ±1SD، ±2SD، ±3SD با رنگهای متفاوت مشخص شوند.
5. تحلیل نمودار در کنترل کیفی آزمایشگاه:
– اگر نتایج بین ±2SD هستند → سیستم پایدار است.
– اگر از ±2SD یا ±3SD خارج شوند → باید با قوانین وستگارد تحلیل شوند.
مثال عددی:
میانگین کنترل: 100، SD=2
→ محدودهها:
– ±1SD = 98–102
– ±2SD = 96–104
– ±3SD = 94–106
اگر مقدار کنترل 107 بهدست آید → خارج از 3SD → خطای تصادفی محتمل است و باید در چارچوب کنترل کیفی آزمایشگاه بررسی شود.
بخش ۶: قوانین وستگارد (Westgard Rules)
قوانین وستگارد مجموعهای از معیارهای آماری برای تفسیر نتایج کنترل کیفی است. این قوانین کمک میکنند خطاهای تصادفی (Random) و سیستماتیک (Systematic) شناسایی شوند و نقش مهمی در تفسیر نمودار لویجنینگ و کنترل کیفیت آزمایشگاه دارند.
| قانون | توضیح | نوع خطا | مثال عددی (Mean=100, SD=2) | اقدام اصلاحی |
|---|---|---|---|---|
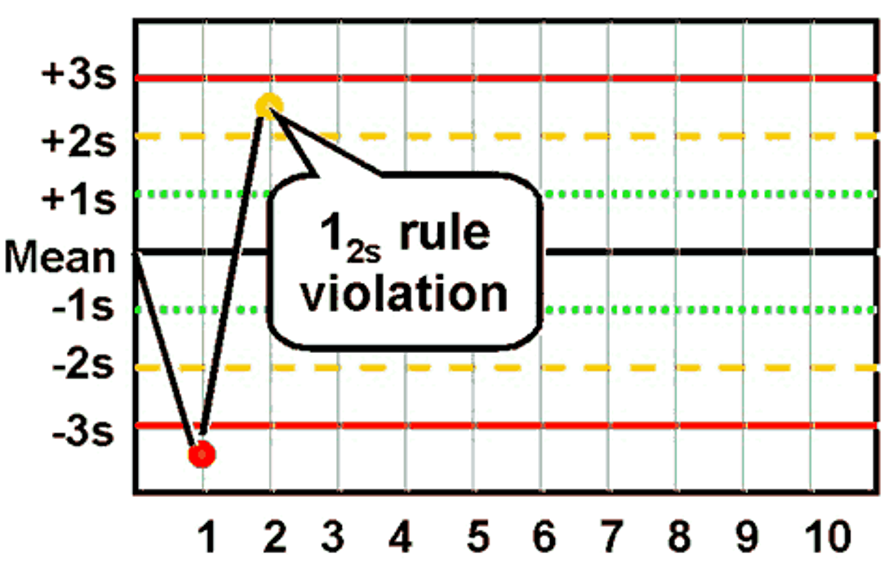
| 1₍₂S₎ | یک کنترل خارج از ±2SD | هشدار | نتیجه 104 یا 96 | بررسی بیشتر، هنوز رد نشود |
| 1₍₃S₎ | یک کنترل خارج از ±3SD | تصادفی | نتیجه 107 یا 93 | رد سری، تکرار تست |
| 2₍₂S₎ | دو کنترل متوالی در یک جهت خارج از ±2SD | سیستماتیک | دو روز 104 و 105 | بررسی کالیبراسیون |
| R₍₄S₎ | اختلاف دو کنترل در یک نوبت بیش از 4SD | تصادفی | یکی 106، دیگری 94 | بررسی خطای نمونهگیری |
| 4₍₁S₎ | چهار کنترل متوالی خارج از ±1SD در یک جهت | سیستماتیک | 101،102،102،103 | بررسی معرف یا دستگاه |
| 10₍x₎ | ده کنترل متوالی در یک طرف میانگین | سیستماتیک | همه بین 101–103 | تنظیم مجدد دستگاه |
| 7₍x₎ | هفت کنترل متوالی در یک طرف میانگین | سیستماتیک | نتایج 99 تا 101 | بررسی روند تدریجی خطا |
| 8₍x₎ | هشت کنترل متوالی در یک طرف میانگین | سیستماتیک | نتایج 101 تا 104 | مشابه 10x، بررسی Bias |
| 12₍x₎ | دوازده کنترل متوالی در یک سمت میانگین | سیستماتیک | نتایج پیوسته بالاتر از Mean | بررسی کالیبراسیون |
| 9₍x₎ | نه کنترل متوالی در یک جهت خاص | سیستماتیک | نتایج همگی پایینتر از Mean | بازبینی روش و دستگاه |
نکته:
قوانین 1₍₂S₎ و 1₍₃S₎ معمولاً بهعنوان “قانون هشدار” و سایر قوانین بهعنوان “قوانین رد” شناخته میشوند.
در صورت نقض هر قانون، باید اقدامات اصلاحی (Corrective Actions) انجام شود و تا رفع مشکل، نتایج بیماران گزارش نشود. استفاده صحیح از این قوانین، از ارکان اصلی کنترل کیفی آزمایشگاه است.
جهت مطالعه ی جامع در مورد قوانین وستگارد و نمودار لوی جنینگ به لینک زیر مراجعه کنید:
قوانین وستگارد چیست؟ راهنمای کامل کنترل کیفی داخلی و نمودار لوی جنینگ در آزمایشگاه
بخش ۷: تحلیل خطاها و اقدامات اصلاحی
خطاها بهصورت کلی به دو دسته خطاهای تصادفی و خطاهای سیستماتیک تقسیم میشوند. تشخیص نوع خطا برای انتخاب اقدام اصلاحی مناسب ضروری است.
خطاهای تصادفی (Random Errors)
علتها:
– نوسان دما
– خطای پیپت
– حباب در کووت
– نوسان برق دستگاه
اقدام: تکرار کنترل، بررسی تجهیزات، حذف حبابها، کنترل شرایط محیطی.
خطاهای سیستماتیک (Systematic Errors)
علتها:
– کالیبراسیون اشتباه
– معرف معیوب
– خرابی دستگاه
اقدام: بررسی Calibration، جایگزینی معرف، سرویس دستگاه، بررسی Bias در کنترل کیفی آزمایشگاه.
هرگاه یکی از قوانین وستگارد نقض شود، تا زمان شناسایی علت و انجام اقدام اصلاحی، نباید نتایج بیماران گزارش شود. این اصل، هستهی ایمنی بیمار در کنترل کیفی آزمایشگاه است.
بخش ۸: کنترل کیفی خارجی (External Quality Assessment – EQA/PT) در آزمایشگاه تشخیصی
در این سیستم، مرکز ارزیابی (مثلاً انستیتو پاستور یا WHO) نمونههایی را به آزمایشگاه ارسال میکند.
آزمایشگاه نتایج را گزارش میکند و مرکز، عملکرد آزمایشگاه را با میانگین گروه مقایسه میکند. این فرآیند بخشی مکمل برای کنترل کیفی آزمایشگاه است و صحت کلی عملکرد را نشان میدهد.
تحلیل:
اگر Bias آزمایشگاه بیش از 5% باشد → نیاز به بررسی مجدد روش و کالیبراسیون است.
نتایج EQA میتوانند خطاهایی را آشکار کنند که در IQC روزانه دیده نمیشوند.
بخش ۹: مستندسازی و بازنگری
تمام دادههای کنترل، اقدامات اصلاحی، و نتایج EQA باید نگهداری و دورهای بازنگری شوند.
تحلیل آماری فصلی میتواند روندهای خطا را مشخص کند و از بروز مجدد آنها پیشگیری نماید.
جمعبندی
کنترل کیفی در آزمایشگاه تشخیص پزشکی نه یک کار روزمره، بلکه پایهی اعتماد به نتایج آزمایشگاهی است.
اجرای دقیق کنترل کیفی داخلی، تحلیل نمودارهای لویجنینگ بر اساس قوانین وستگارد، و مشارکت همهی پرسنل در سیستم مدیریت کیفیت، تضمینکنندهی اعتبار علمی هر آزمایشگاه است.
سوالات متداول
۱. کنترل کیفی در آزمایشگاه چیست و چه اهمیتی دارد؟
کنترل کیفی در آزمایشگاه مجموعهای از فعالیتهاست که با هدف پایش دقت و صحت نتایج آزمایشها انجام میشود. اهمیت آن در این است که بدون کنترل کیفیت، نتایج میتوانند گمراهکننده باشند و تصمیمات بالینی اشتباه بهدنبال داشته باشند.
۲. تفاوت QA و QC در آزمایشگاه تشخیص پزشکی چیست؟
QA یا تضمین کیفیت، چارچوب کلی و برنامهریزیشده برای مدیریت کیفیت در آزمایشگاه است، در حالی که QC بخشی از QA بوده و بر پایش روزانه صحت و دقت نتایج تمرکز دارد. بهعبارت ساده، QC ابزار اجرایی در دل سیستم QA است.
۳. چرا استفاده از نمودار لویجنینگ در کنترل کیفی ضروری است؟
نمودار لویجنینگ امکان مشاهده روند نتایج کنترل در طول زمان را فراهم میکند. با این نمودار میتوان تغییرات تدریجی، جهشی یا الگوهای خاص خطا را تشخیص داد و قبل از تأثیر بر نتایج بیماران، اقدامات اصلاحی را انجام داد.
۴. چند بار در روز باید کنترل کیفی داخلی (IQC) انجام شود؟
بسته به نوع تست و حجم کاری، معمولاً در هر شیفت کاری حداقل یک بار باید IQC انجام شود. در تستهای بحرانی یا دستگاههای پرکار، ممکن است نیاز به کنترل بیشتر (مثلاً هر چند ساعت یکبار) وجود داشته باشد.
۵. در صورت نقض قوانین وستگارد چه باید کرد؟
در صورت نقض قوانین وستگارد، ابتدا باید آزمایش کنترل تکرار شود. اگر خطا تأیید شد، باید کالیبراسیون، معرفها، دستگاه و شرایط محیطی بررسی شوند و تا زمان حل مشکل، گزارش نتایج بیماران متوقف شود.
۶. تفاوت خطای تصادفی و سیستماتیک چیست؟
خطای تصادفی بهصورت پراکندگی غیرمنظم نتایج حول میانگین دیده میشود، در حالیکه خطای سیستماتیک بهصورت انحراف ثابت و جهتدار از مقدار واقعی است. خطای سیستماتیک معمولاً ناشی از کالیبراسیون اشتباه یا معرف معیوب است.
۷. نقش کنترل کیفی خارجی (EQA/PT) در آزمایشگاه چیست؟
کنترل کیفی خارجی عملکرد کلی آزمایشگاه را با سایر آزمایشگاهها مقایسه میکند. این ارزیابی کمک میکند تا خطاهایی که در کنترل داخلی دیده نمیشوند، شناسایی شده و اصلاح شوند.
۸. چه زمانی نیاز به اعتبارسنجی مجدد یک روش آزمایشگاهی داریم؟
هنگام تعویض معرف، تغییر دستگاه، تغییر عمده در روش، یا مشاهدهی تغییرات غیرقابل توجیه در کنترلها، لازم است اعتبارسنجی مجدد یا حداقل ارزیابی بخشی از پارامترهای عملکردی انجام شود.
۹. چرا مستندسازی در کنترل کیفی اهمیت دارد؟
مستندسازی امکان پیگیری خطاها، بررسی روندها و ارائه شواهد برای ممیزیها و اعتباربخشی را فراهم میکند. بدون مستندسازی، حتی سیستمهای خوب کنترل کیفیت نیز از دید نهادهای ناظر نامعتبر بهنظر میرسند.
۱۰. چه عواملی میتوانند باعث شکست سیستم کنترل کیفی شوند؟
عدم آموزش کافی پرسنل، بیتوجهی به نتایج کنترل، نادیده گرفتن قوانین وستگارد، استفاده از معرفهای تاریخگذشته، و فقدان QMS مؤثر میتوانند باعث شکست سیستم کنترل کیفی آزمایشگاه شوند. پیشگیری از این عوامل نیازمند فرهنگ کیفیت و مدیریت قوی است.
منابع معتبر
- Westgard JO. Basic QC Practices, 5th Edition, Westgard QC, 2023.
لینک:
وبسایت Westgard QC
- WHO. Laboratory Quality Management System Handbook, 2022.
لینک:
CLSI C24
- ISO 15189: Medical Laboratories – Requirements for Quality and Competence, 2022.
لینک:
ISO 15189
