دیسک آنتی بیوگرام: راهنمای جامع تست حساسیت آنتی بیوتیکی
خلاصه: تست دیسک آنتی بیوگرام (Kirby-Bauer) روشی استاندارد برای بررسی حساسیت باکتری ها به آنتی بیوتیکهاست. دیسکهای حاوی دارو روی Mueller-Hinton agar قرار گرفته و قطر ناحیه بدون رشد تفسیر میشود. این تست برای باکتریهای گرم مثبت و منفی کاربرد دارد.
فهرست مطالب
- مقدمه — دیسک آنتی بیوگرام و انتخاب محیط کشت (Mueller-Hinton)
- دیسکهای آنتی بیوگرام برای باکتریهای گرم مثبت — آنتیبیوتیکها و نکات
- دیسکهای آنتی بیوگرام برای باکتریهای گرم منفی — مقاومتها و تستهای تکمیلی
- حدود دیسکهای آنتی بیوگرام (Zone Diameters) — جداول و مرجع
- تفسیر تست آنتیبیوگرام — S, I, R و کاربرد بالینی
- محدودیتهای دیسک آنتی بیوگرام
- مخفف دیسکهای آنتی بیوگرام
- اهمیت بالینی و مقاومت آنتیبیوتیکی (AMR)
- نتیجهگیری
- سوالات رایج (FAQ)
مقدمه — دیسک آنتی بیوگرام و انتخاب محیط کشت (Mueller-Hinton)
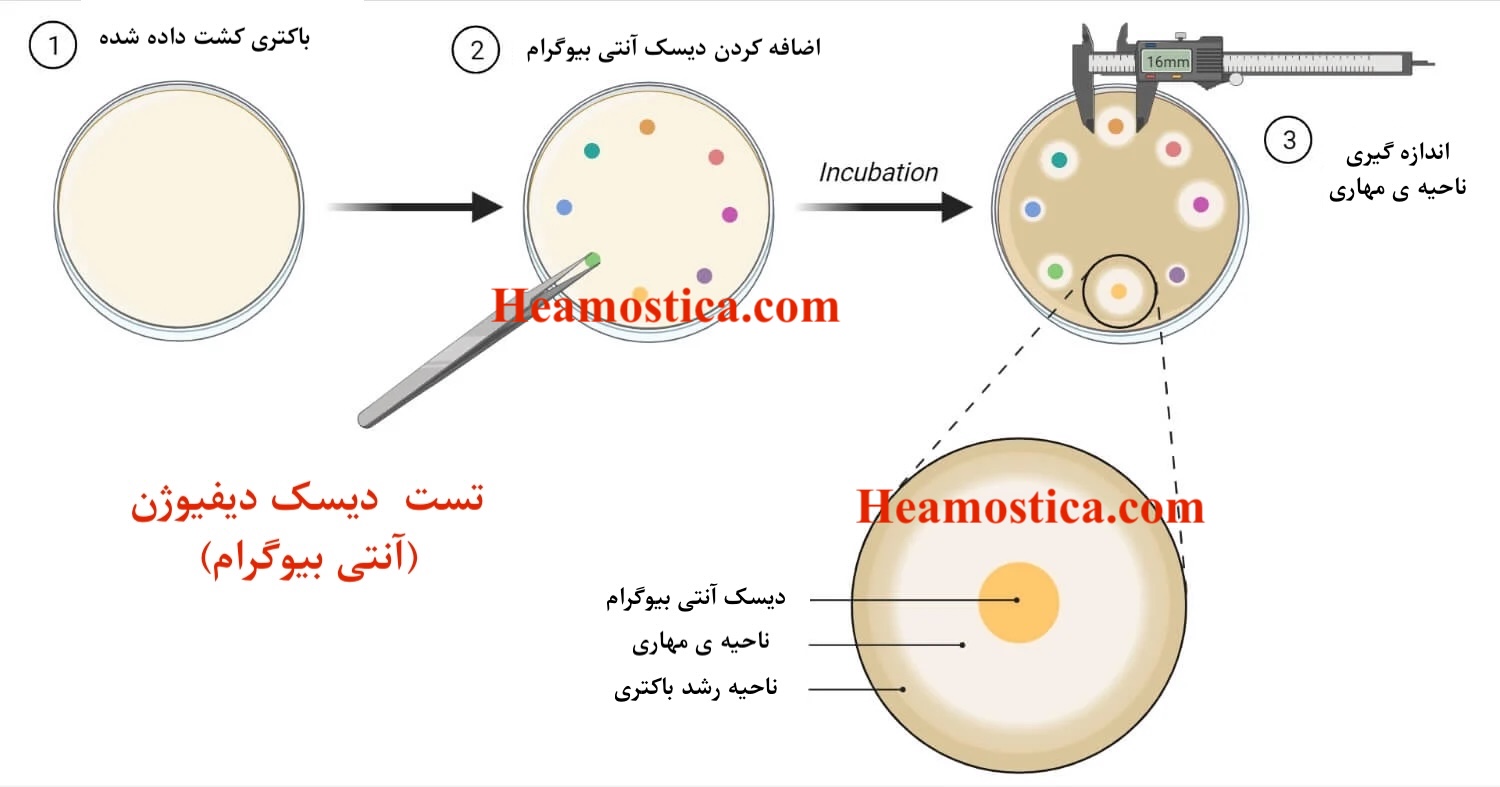
تست دیسک دیفیوژن یا روش Kirby-Bauer، یک روش استاندارد و پرکاربرد در آزمایشگاههای میکروبیولوژی است که برای تعیین حساسیت یا مقاومت باکتریها به آنتیبیوتیکها به کار میرود. در این روش، دیسکهای کاغذی حاوی غلظت مشخصی از آنتیبیوتیک روی سطح Mueller-Hinton agar (MHA) که با باکتری کشت داده شده قرار میگیرند. پس از انکوباسیون در دمای 35–37 درجه سانتیگراد به مدت 18–24 ساعت، ناحیهای شفاف اطراف دیسک (zone of inhibition) تشکیل میشود که اندازه آن بهعنوان شاخص حساسیت باکتری به آنتیبیوتیک مورد استفاده قرار میگیرد.
چرا Mueller-Hinton Agar؟
این محیط به عنوان استاندارد طلایی انتخاب شده است زیرا:
- ترکیب یکنواخت و پایدار دارد.
- pH کنترلشده (7.2–7.4) و ضخامت استاندارد (4 میلیمتر) دارد.
- فاقد مواد مهارکننده است و به رشد اکثر باکتریهای هوازی غیر فاستیدیوس کمک میکند.
- انتشار آنتیبیوتیکها در آن یکنواخت و قابل پیشبینی است.
استثناها
با وجود این، برخی باکتریهای فاستیدیوس نیاز به محیطهای غنیتر یا اختصاصی دارند:
- استرپتوکوکها و پنوموکوکها: Mueller-Hinton + 5% خون گوسفند
- Haemophilus influenzae: Haemophilus Test Medium (HTM)
- Neisseria gonorrhoeae: GC agar با مکملهای تغذیهای
- باکتریهای بیهوازی: دیسک دیفیوژن مناسب نیست؛ روشهای MIC استفاده میشوند.
دیسکهای آنتی بیوگرام برای باکتریهای گرم مثبت — آنتیبیوتیکها و نکات
باکتریهای گرم مثبت شامل گونههای مهمی مانند Staphylococcus aureus، Streptococcus spp. و Enterococcus spp. هستند. برای این دسته از باکتریها، دیسکهای انتخابی بر اساس استانداردهای CLSI طراحی میشوند. برخی از آنتیبیوتیکهای رایج در تست گرم مثبتها عبارتند از:
- پنیسیلین (P) – تست اولیه حساسیت به بتالاکتامها
- وانکومایسین (VA) – برای شناسایی سویههای مقاوم مانند MRSA
- اریترومایسین (E) – تست حساسیت ماکرولیدها
- کلندامایسین (CC) – بهویژه در استافیلوکوکها (با تست D-zone برای مقاومت القایی)
- تتراسایکلین (TE) – با طیف وسیعتر
- کلرامفنیکل (C) – به عنوان گزینه جایگزین در مقاومتهای چندگانه
برای این تستها، معمولاً از دیسکهای با غلظت استاندارد استفاده میشود (مانند پنیسیلین 10U، وانکومایسین 30 µg). نتایج باید با جداول CLSI یا EUCAST مقایسه شوند. میزان توافق این روش با روشهای رقیقسازی (broth microdilution) برای گرم مثبتها بالاست (حدود 85–90%).
دیسکهای آنتی بیوگرام برای باکتریهای گرم منفی — مقاومتها و تستهای تکمیلی
باکتریهای گرم منفی از نظر بالینی بسیار اهمیت دارند زیرا مقاومت دارویی در آنها شایعتر است. مهمترین گروهها شامل Enterobacterales (اشرشیا کلی، کلیبسیلا، انتروباکتر)، Pseudomonas aeruginosa، Acinetobacter spp. و Haemophilus influenzae هستند.
آنتیبیوتیکهای رایج مورد استفاده در تست حساسیت گرم منفیها عبارتند از:
- سفالوسپورینها: سفوتاکسیم (CTX, 30 µg)، سفتازیدیم (CAZ, 30 µg)، سفپیم (FEP, 30 µg)
- آمینوگلیکوزیدها: آمیکاسین (AK, 30 µg)، جنتامایسین (GM, 10 µg)
- فلوروکینولونها: سیپروفلوکساسین (CIP, 5 µg)
- بتالاکتام/بتالاکتاماز اینهیبیتورها: پیپراسیلین/تازوباکتام (TZP, 100/10 µg)
- کارباپنمها: ایمیپنم (IPM, 10 µg)، مروپنم (MEM, 10 µg)
نکته کلیدی
در باکتریهای گرم منفی باید به مقاومتهای اکتسابی توجه ویژه داشت:
- تولید ESBL (Extended Spectrum Beta-Lactamases): منجر به مقاومت به سفالوسپورینهای نسل سوم.
- تولید کارباپنماز (KPC, NDM, OXA-48 و غیره): مقاومت به کارباپنمها.
- مقاومت چندگانه (MDR, XDR, PDR): یکی از چالشهای اصلی درمانی.
برای تشخیص این مقاومتها، تستهای تکمیلی مانند تست ترکیبی دیسک (Double Disk Synergy Test) یا تست کارباپنماز (Modified Hodge Test, Carba NP) در کنار دیسک دیفیوژن استفاده میشوند.
حدود دیسکهای آنتی بیوگرام (Zone Diameters) — جداول و مرجع
قطر zone بر اساس جداول CLSI یا EUCAST تفسیر میشود و سه دسته حساس (S)، متوسط حساس (I)، و مقاوم (R) را مشخص میکند.
مثال: استافیلوکوکوس اورئوس (CLSI 2022):
| آنتیبیوتیک | مخفف | غلظت دیسک | حساس (S) ≥ mm | متوسط (I) mm | مقاوم (R) ≤ mm |
|---|---|---|---|---|---|
| پنیسیلین | P | 10 U | 29 | – | 28 |
| وانکومایسین | VA | 30 µg | 15 | 11–14 | ≤10 |
| اریترومایسین | E | 15 µg | 23 | 14–22 | ≤13 |
| کلندامایسین | CC | 2 µg | 21 | 15–20 | ≤14 |
| تتراسایکلین | TE | 30 µg | 19 | 15–18 | ≤14 |
⚠️ این حدود برای هر گونه و هر آنتیبیوتیک متفاوت است و باید همیشه با آخرین نسخه CLSI (M100) یا EUCAST تطبیق داده شود.
جهت مطالعه جامع در مورد کنترل کیفی میکروبیولوژی به لینک زیر مراجعه کنید:
کنترل کیفی میکروب شناسی: اصول، روشها و استانداردهای عملکرد
تفسیر تست آنتیبیوگرام — S, I, R و کاربرد بالینی
نتایج بر اساس قطر ناحیه مهار رشد تفسیر میشوند:
- حساس (S): درمان با دوز استاندارد مؤثر خواهد بود.
- متوسط حساس (I): اثر دارو در دوزهای بالاتر یا در شرایط خاص (مثل غلظت بالای ادرار) قابل انتظار است.
- مقاوم (R): درمان با آن دارو مؤثر نخواهد بود.
تفسیر نتایج باید با شرایط بالینی بیمار (محل عفونت، دوز دارو، سن، بیماریهای زمینهای) همراه باشد.
محدودیتهای دیسک آنتی بیوگرام
هرچند تست دیسک دیفیوژن مزایایی مانند سادگی و هزینه کم دارد، اما محدودیتهایی نیز وجود دارد:
- عدم تعیین MIC دقیق (فقط کیفی است).
- نتایج غیرقابل اعتماد برای برخی داروها (مثلاً آمینوگلیکوزیدها).
- نامناسب برای باکتریهای بیهوازی و کندرشد.
- حساس به عوامل محیطی (pH، ضخامت آگار، کیفیت دیسکها).
مخفف دیسکهای آنتی بیوگرام
در تستهای حساسیت، دیسکها با مخففهای استانداردی برچسبگذاری میشوند تا شناسایی آسان باشد. بر اساس CLSI و EUCAST، برخی مخففهای رایج عبارتند از:
| نام کامل آنتیبیوتیک | مخفف | غلظت رایج (μg) |
|---|---|---|
| آموکسیسیلین | AML | 20 |
| آگمنتین (آمپیسیلین/سولباکتام) | AMC | 20/10 |
| آمیکاسین | AK | 30 |
| باسیتراسین | B | 10 U |
| سفپیم | FEP | 30 |
این مخففها در کارتریجهای دیسک (مانند Bio-Rad) استفاده میشوند و EUCAST سیستم یکپارچهای برای اختصارات ارائه میدهد.
اهمیت بالینی و مقاومت آنتیبیوتیکی (AMR)
آنتیبیوگرام یکی از ابزارهای اصلی در برنامههای کنترل مقاومت آنتیبیوتیکی (Antimicrobial Stewardship Programs) است. نتایج صحیح و بهروز آن به پزشکان کمک میکند درمانهای هدفمندتر انتخاب کنند و از مصرف بیرویه آنتیبیوتیکها جلوگیری شود. به همین دلیل، آزمایشگاهها باید همیشه آخرین دستورالعملهای CLSI و EUCAST را دنبال کنند.
نتیجهگیری
تست دیسک دیفیوژن ابزاری ساده، ارزان و قابل اعتماد برای تعیین حساسیت باکتریهاست. اگرچه محدودیتهایی دارد، اما همچنان بهعنوان یکی از ستونهای اصلی آزمایشگاههای میکروبیولوژی باقی مانده است. برای موارد خاص، ترکیب آن با روشهای MIC و تستهای مولکولی توصیه میشود.
سوالات رایج (FAQ)
1. دیسک آنتی بیوگرام چیست؟
دیسک آنتی بیوگرام روشی آزمایشگاهی برای بررسی حساسیت باکتریها به آنتیبیوتیکها با استفاده از دیسکهای کاغذی آغشته به دارو است.
2. تست Kirby-Bauer چه تفاوتی با دیگر روشها دارد؟
تست Kirby-Bauer یک روش دیسک دیفیوژن استاندارد است که به دلیل سادگی و هزینه کم برای ارزیابی اولیه حساسیت باکتریها استفاده میشود.
3. چرا از دیسک آنتی بیوگرام برای باکتریهای گرم مثبت استفاده میشود؟
دیسک آنتی بیوگرام برای باکتریهای گرم مثبت به دلیل اثربخشی آنتیبیوتیکهایی مانند پنیسیلین و وانکومایسین علیه دیواره سلولی این باکتریها استفاده میشود.
4. چگونه نتایج تست آنتی بیوگرام تفسیر میشود؟
نتایج بر اساس قطر ناحیه بدون رشد (zone diameter) به سه دسته حساس (S)، متوسط (I) و مقاوم (R) تقسیم میشوند.
5. استاندارد CLSI چیست؟
CLSI مجموعه استانداردهایی برای تستهای حساسیت آنتیبیوتیکی ارائه میدهد که حدود zone diameter و روشهای تست را مشخص میکند.
6. آیا دیسک آنتی بیوگرام برای باکتریهای بیهوازی مناسب است؟
خیر، این روش برای باکتریهای بیهوازی مناسب نیست و نیاز به روشهای دیگر مانند تستهای رقیقسازی دارد.
7. مخففهای دیسک آنتی بیوگرام چه معنایی دارند؟
مخففها مانند P (پنیسیلین)، VA (وانکومایسین) و E (اریترومایسین) برای شناسایی سریع آنتیبیوتیکها در تست استفاده میشوند.
8. چرا محیط Mueller-Hinton در تست دیسک دیفیوژن استفاده میشود؟
این محیط به دلیل ترکیب استاندارد و توانایی پشتیبانی از رشد باکتریها و انتشار یکنواخت آنتیبیوتیک مناسب است.
9. آیا تست دیسک آنتی بیوگرام MIC را مشخص میکند؟
خیر، این تست کیفی است و برای تعیین MIC دقیق نیاز به روشهای دیگر مانند E-test است.
10. چه عواملی میتوانند نتایج تست دیسک آنتی بیوگرام را تحت تأثیر قرار دهند؟
عواملی مانند pH محیط، ضخامت آگار، زمان انکوباسیون و کیفیت دیسکها میتوانند نتایج را تغییر دهند.
11. چه ارگانیسمهایی نیاز به محیط کشت اختصاصی دارند؟
استرپتوکوکها و پنوموکوکها اغلب نیاز به Mueller-Hinton با 5% خون گوسفند دارند؛ Haemophilus نیاز به HTM دارد؛ و Neisseria ممکن است نیاز به GC agar داشته باشد.
12. چه مواردی نیاز به تست تکمیلی دارند؟
شناسایی ESBL و کارباپنماز معمولاً نیاز به تستهای تکمیلی (مانند Double Disk Synergy، Carba NP) دارند تا مقاومتهای خاص را تأیید کنند.
جهت مطالعه بیشتر به لینک زیر مراجعه کنید: