فهرست مطالب
اهداف یادگیری
در پایان این فصل، دانشجو قادر خواهد بود:
- فرآیند تولید (هماتوپوئیز) گلبول های سفید و پلاکتها را از سلولهای بنیادی اولیه تا فرمهای بالغ و تخصصیشان تشریح کنید.
- پیچیدگیهای تمایز انواع مختلف گلبول های سفید (مانند نوتروفیلها، لنفوسیتها، مونوسیتها، ائوزینوفیلها و بازوفیلها) را درک کنید.
- عملکرد حیاتی هر یک از انواع گلبول های سفید و پلاکتها را در سیستم ایمنی بدن و فرآیند هموستاز توضیح دهید.
- انواع مختلف گلبول های سفید را از نظر مورفولوژیک در زیر میکروسکوپ شناسایی کنید.
- نقش فاکتورهای رشد و سیتوکینهای مختلف را در تولید و تمایز گلبول های سفید و پلاکتها بیان کنید.
- مفهوم شیفت به چپ نوتروفیلی و اهمیت آن در تشخیص بالینی را توضیح دهید.
- ویژگیهای کینتیکی و توزیع گلبول های سفید و پلاکتها در بدن را تحلیل کنید.
- اهمیت بالینی تغییرات در تعداد و مورفولوژی گلبول های سفید و پلاکتها را در بیماریهای مختلف درک کنید.
جهت عضویت در کانال آموزشی در تلگرام به لینک زیر مراجعه کنید:
https://t.me/hematology_education
مقدمه
در دنیای پیچیده و حیرتانگیز بدن انسان، سیستمی بیوقفه و دقیق در حال فعالیت است که وظیفه حفاظت و ترمیم را بر عهده دارد. فصل چهارم از دوره آموزشی ما به دو جزء حیاتی از این سیستم، یعنی گلبول های سفید (لکوسیتها) و پلاکتها (ترومبوسیتها)، اختصاص دارد. این ذرات میکروسکوپی، با وجود ابعاد کوچکشان، نقشهای بسیار بزرگی در حفظ سلامت و بقای ما ایفا میکنند.
در این فصل، ما سفری به عمق مغز استخوان خواهیم داشت؛ جایی که این سلولهای شگفتانگیز متولد میشوند و فرآیند تولید (هماتوپوئیز) آنها را از سلولهای بنیادی اولیه تا فرمهای بالغ و تخصصیشان دنبال خواهیم کرد. همچنین، به بررسی پیچیدگیهای تمایز آنها خواهیم پرداخت و خواهیم دید که چگونه یک سلول بنیادی قادر است به انواع مختلفی از گلبول های سفید (مانند نوتروفیلها، لنفوسیتها، مونوسیتها، ائوزینوفیلها و بازوفیلها) تبدیل شود که هر یک وظایف منحصر به فردی در سیستم ایمنی بر عهده دارند.
در ادامه، بر عملکرد حیاتی این سلولها تمرکز خواهیم کرد. گلبول های سفید، سربازان خط مقدم بدن ما هستند که با شناسایی و نابودی عوامل بیماریزا نظیر باکتریها، ویروسها، قارچها و سلولهای سرطانی، ما را در برابر عفونتها و بیماریها محافظت میکنند. از سوی دیگر، پلاکتها، ترمیمکنندگان چابک بدن به شمار میروند که با تشکیل لختههای خونی، جلوی خونریزی را گرفته و به بازسازی بافتهای آسیبدیده کمک میکنند.
درک عمیق از تولید، تمایز و عملکرد گلبول های سفید و پلاکتها نه تنها برای دانشجویان علوم آزمایشگاهی از اهمیت بالایی برخوردار است، بلکه به آنها کمک میکند تا نقش حیاتی خود را در تشخیص و پایش بیماریهای مرتبط با خون و سیستم ایمنی به بهترین نحو ایفا کنند. با ما همراه باشید تا پرده از اسرار این اجزای شگفتانگیز بدن برداریم.
نوتروفیلها: خط مقدم دفاعی بدن
نوتروفیلها، فراوان ترین نوع گلبول های سفید، نقش حیاتی در سیستم ایمنی بدن ایفا میکنند. این سلولها به عنوان اولین خط دفاعی در برابر عوامل بیماریزا عمل کرده و با شناسایی و از بین بردن مهاجمان، به حفظ سلامت بدن کمک میکنند. در ادامه به بررسی تولید، تمایز و عملکرد نوتروفیلها میپردازیم.
تولید و تمایز نوتروفیلها: سفری از مغز استخوان تا خون
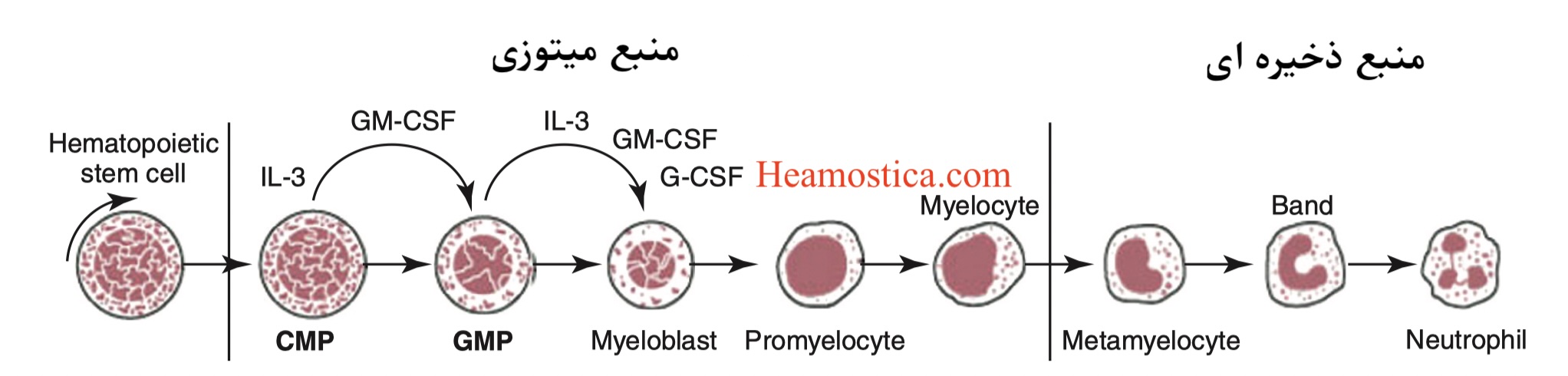
تولید نوتروفیلها، فرآیندی پیچیده به نام گرانولوپوئز، از سلولهای بنیادی خونساز در مغز استخوان آغاز میشود و حدود 14 روز به طول میانجامد. این فرآیند تحت تأثیر فاکتورهای رشد مختلفی از جمله G-CSF (مهمترین فاکتور رشد در تمایز نوتروفیلها)، GM-CSF و IL-3 انجام میپذیرد.
مسیر تمایز نوتروفیلها به شرح زیر است:
- سلول بنیادی خونساز (HSC): نقطه آغازین تولید تمام سلولهای خونی.
- پروژنیتور مشترک میلوئیدی (CMP یا CFU-GEMM): HSC تحت تأثیر IL-3 به CMP تبدیل میشود.
- پروژنیتور گرانولوسیت-مونوسیت (GMP): CMP تحت تأثیر GM-CSF به GMP تبدیل میشود.
- میلوبلاست: GMP تحت تأثیر G-CSF، GM-CSF و IL-3 به اولین پیشساز متعهد رده نوتروفیلی، یعنی میلوبلاست، تبدیل میشود. میلوبلاست اولین سلولی است که از نظر مورفولوژیک زیر میکروسکوپ نوری قابل تشخیص است. این سلول حدود 15 میکرومتر قطر دارد، هسته بیضی تا چهار گوش با کروماتین ظریف و 2 تا 5 هستک دارد و سیتوپلاسم آن آبی شفاف است. از نظر ایمنوفنوتایپ، میلوبلاستها +CD13/33+, CD34+, CD15/117+, HLA-DR+ هستند.
- پرومیلوسیت: میلوبلاست پس از یک تقسیم میتوز، دو سلول بزرگتر به نام پرومیلوسیت تولید میکند. در این مرحله، هسته اندکی به کنار میرود، کروماتین هسته خشنتر میشود و هستکها تقریباً ناپدید میشوند. سیتوپلاسم بازوفیلیک بوده و عمدتاً توسط گرانولهای آزوروفیلیک (اولیه) پوشیده شده است. این گرانولها حاوی آنزیمهای لیزوزومی (مانند اسید فسفاتاز)، الاستاز، میلوپراکسیداز (MPO) و پروتئینهای کاتیونی ضد باکتریایی (مانند دیفنسین و کاتپسین) هستند.
- میلوسیت: پرومیلوسیت پس از تقسیم میتوز به میلوسیت تبدیل میشود. ظهور گرانولهای اختصاصی (ثانویه) مشخصه این مرحله است که به فاکتور رونویسی C/EBPε وابسته است. نقص در ژن C/EBPε منجر به بیماری نقص گرانولهای اختصاصی (SGD) و عفونتهای مکرر میشود. گرانولهای اختصاصی حاوی پروتئینهای ضد باکتریایی مانند لیزوزیم و لاکتوفرین هستند. میلوسیت آخرین مرحلهای است که سلول توانایی تقسیم دارد.
- متامیلوسیت: متامیلوسیتها طی 1 تا 3 تقسیم از میلوسیتها به وجود میآیند و توانایی تقسیم میتوزی ندارند. هسته این سلولها فرورفته (لوبیا یا کلیوی شکل) و کروماتین متراکم است. متامیلوسیتها CD16 را بیان میکنند که مارکر مخصوص این مرحله است.
- باند سل (Band cell یا Stab): متامیلوسیت تمایز یافته و به باند سل تبدیل میشود. در این مرحله، هسته دارای کروماتین متراکمتر و شکلی کشیدهتر یا دولوبه پیدا میکند. باند سل اولین سلول رده نوتروفیلی است که در حالت طبیعی وارد خون میشود و حدود 3 درصد نوتروفیلهای خون را تشکیل میدهد.
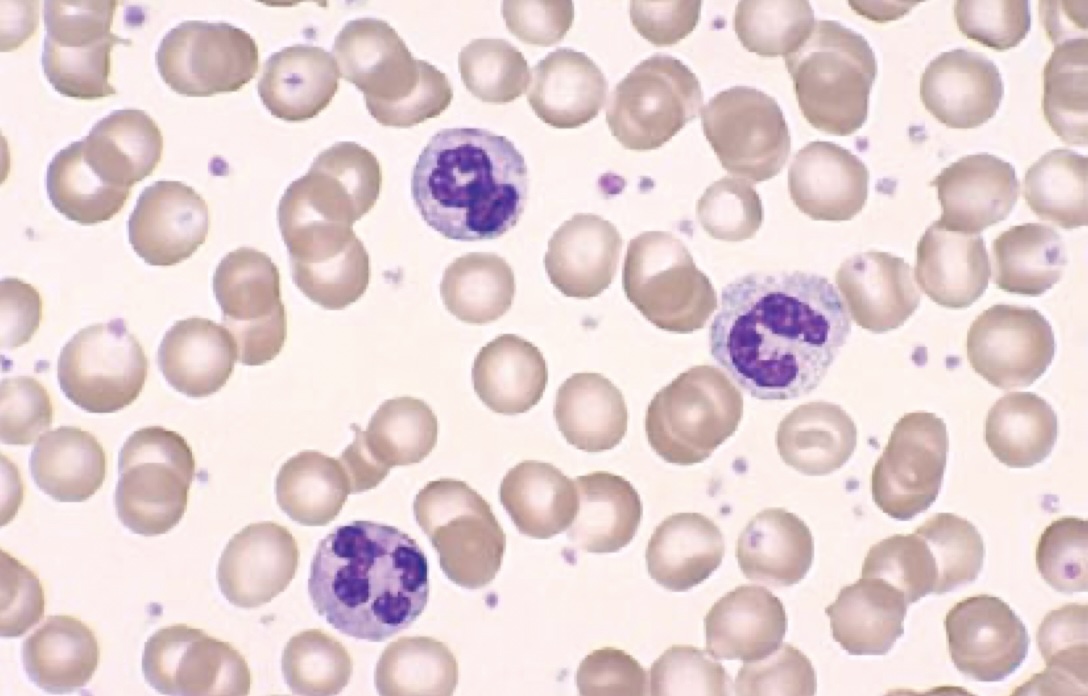
- نوتروفیل بالغ (Segmented): باند سل با ادامه انقباض هسته و ایجاد رشتههای ظریف بین لوبهای هسته، به نوتروفیل بالغ تبدیل میشود. هسته نوتروفیلهای بالغ 2 تا 5 لوب دارد و 40 تا 60 درصد گلبول های سفید را تشکیل میدهند. تشخیص باند از نوتروفیل بر اساس ضخامت پل بین لوبهای هسته انجام میشود؛ اگر فیلامنت نازک باشد نوتروفیل و اگر ضخیم باشد باند است.
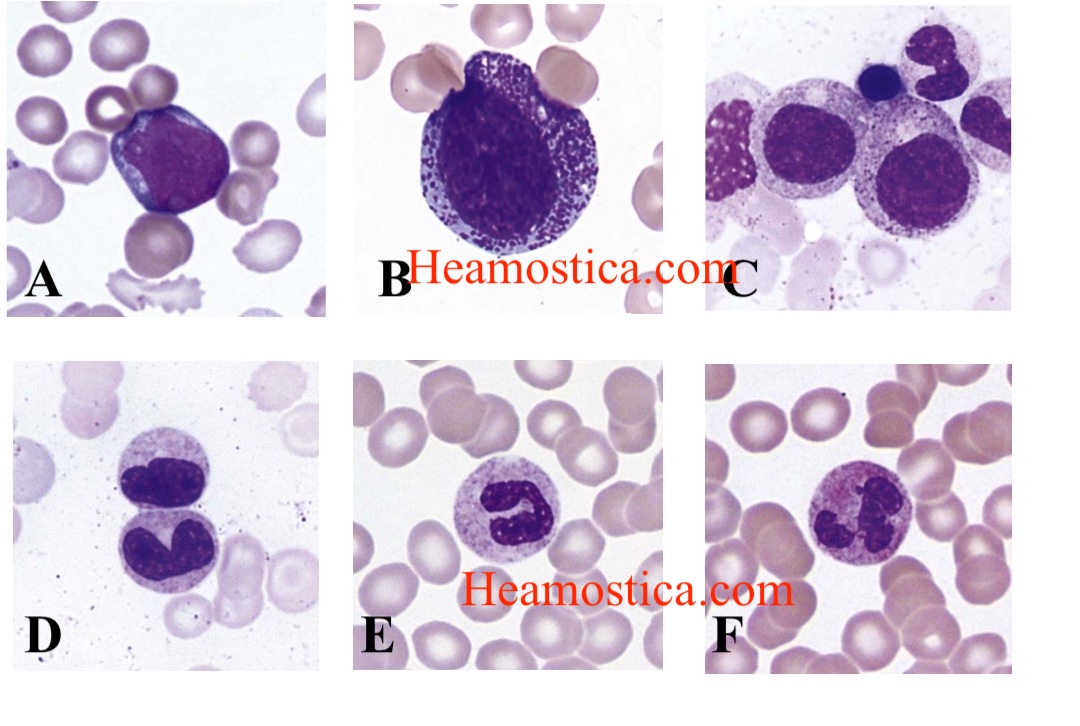
سلول های پیشساز نوتروفیلی. A) میلوبلاست. B) پرومیلوسیت C). میلوسیت D). متامیلوسیت E). سلول باند F) نوتروفیل بالغ
- هیپرسگمنتاسیون: مشاهده 5 درصد یا بیشتر نوتروفیلهای 5 لوبه یا 1 درصد نوتروفیلهای 6 یا 7 لوبه، نشانهای بارز در آنمی مگالوبلاستیک است.
- پلگر هیوت (Pelger-Huët Anomaly): نقص در سگمنتاسیون هسته که بیشتر هستهها دو لوبه باقی میمانند (هیپوسگمنتاسیون).
در شرایط نیاز بالا به نوتروفیل، سرعت تولید آنها افزایش مییابد، اما ممکن است مراحل بلوغ هسته کامل نشود و باند سل و گاهی میلوسیتها وارد خون شوند که به آن شیفت به چپ نوتروفیلی (Shift to Left) یا باندمی میگویند.
توزیع و کینتیک نوتروفیلها
به طور متوسط، از یک میلوبلاست 16 نوتروفیل تولید میشود. نوتروفیلها پس از ورود به خون، بین حوضچه گرانولوسیتی در گردش (CGP) و حوضچه گرانولوسیتی حاشیهای (MGP) حرکت میکنند که میزان نوتروفیل در هر دو حوضچه برابر است. نمونهگیری برای شمارش لکوسیتها از CGP انجام میشود.
نیمهعمر بیولوژیک نوتروفیلها در خون محیطی 6.5 تا 9 ساعت است. در این مدت، نوتروفیلها از دیواره عروق عبور کرده و وارد بافتها میشوند. این مهاجرت تصادفی از طریق دیاپدز (ایجاد پای کاذب) صورت میگیرد. اگر نوتروفیلها در بافتها وارد واکنش التهابی نشوند، پس از 2 تا 5 روز از طریق ترشحات برونش، بزاق و دستگاه گوارش دفع میشوند یا توسط سیستم رتیکلواندوتلیال از بین میروند. استرس و ورزش (تولید اپینفرین) میتوانند باعث جابجایی نوتروفیلها از MGP به CGP شوند.
عملکرد نوتروفیل
نوتروفیلها سلول های اصلی سیستم ایمنی ذاتی هستند. حرکت آنها به سمت بافتها در حالت عادی تصادفی است، اما در هنگام عفونت یا التهاب، به دلیل وجود عوامل کموتاکسی، حرکت آنها جهتدار و مستقیم به سمت محل عفونت میشود. مهمترین گیرندههای کموکاینی نوتروفیلها، CXCR1 و CXCR2 هستند که به IL-8 تولید شده در محل عفونت متصل شده و مهاجرت نوتروفیلها را تحریک میکنند.
نوتروفیلها عوامل عفونی را از طریق اُپسونینها (مانند C3b و IgG که به FcγR نوتروفیل متصل میشوند) شناسایی کرده و آنها را فاگوسیت (بلعیده) میکنند. پس از فاگوسیتوز، نوتروفیلها عامل بیماریزا را از طریق مکانیسمهای زیر از بین میبرند:
- مکانیسمهای بیهوازی: عوامل بیماریزای بلعیدهشده توسط محتویات مترشحه از گرانولهای آزوروفیلیک و اختصاصی نوتروفیلها از بین میروند.
- مکانیسمهای هوازی (انفجار تنفسی): در این مکانیسم، آنزیم NADPH اکسیداز فعال شده و منجر به تبدیل اکسیژن مولکولی (O2) به سوپراکسید (O2-) و در نهایت تولید یونهای هیپوکلریت (OCL-) میشود. این ترکیبات رادیکال آزاد قوی، خاصیت ضد میکروبی دارند.
در خانمها (XX) و مردان مبتلا به سندرم کلاینفلتر (XXY)، یکی از کروموزومهای X به صورت تصادفی غیرفعال میشود. این کروموزوم غیرفعال به صورت زائدهای چسبیده به هسته نوتروفیل دیده میشود که به آن Drumstick، Barr Body یا جسم کروماتینی X میگویند.
ائوزینوفیلها: مبارزان خاص در برابر انگل ها
ائوزینوفیلها یکی دیگر از انواع مهم گلبول های سفید هستند که با وجود فراوانی کم (1 تا 3 درصد از کل گلبول های سفید خون محیطی)، نقشهای تخصصی و حیاتی در پاسخهای ایمنی بدن، به ویژه در برابر عفونتهای انگلی و واکنشهای آلرژیک ایفا میکنند. در ادامه به بررسی دقیق فرآیند تولید، تمایز و عملکرد این سلولهای منحصر به فرد میپردازیم.
تولید و تمایز ائوزینوفیلها: تولد در مغز استخوان
تولید ائوزینوفیلها، مانند سایر سلولهای خونی، در مغز استخوان آغاز میشود. مسیر تمایزی آنها از سلولهای بنیادی خونساز به شرح زیر است:
مسیر پروژنیتوری تولید ائوزینوفیل به صورت زیر است:
سلول بنیادی خون ساز ← CFU- GEMM ← CFU- EO
مراحل پره کورسوری ائوزینوفیل به شرح زیر می باشد
← میلوبلاست ← پرومیلوسیت ← میلوسیت ائوزینوفیل ← متامیلوسیت ائوزینوفیل ← باند ائوزینوفیل
نهایتا باند ائوزینوفیلی به ائوزینوفیل تبدیل می شود.
سه فاکتور رشد IL- 5 و IL- 3 و GM- CSF و در تمایز ائوزینوفیل نقش دارند.
IL- 5 مهم ترین فاکتور رشد ائوزینوفیل است و از آپوپتوز آن ها جلوگیری می کند و عملکرد آن ها را ارتقا می دهد.
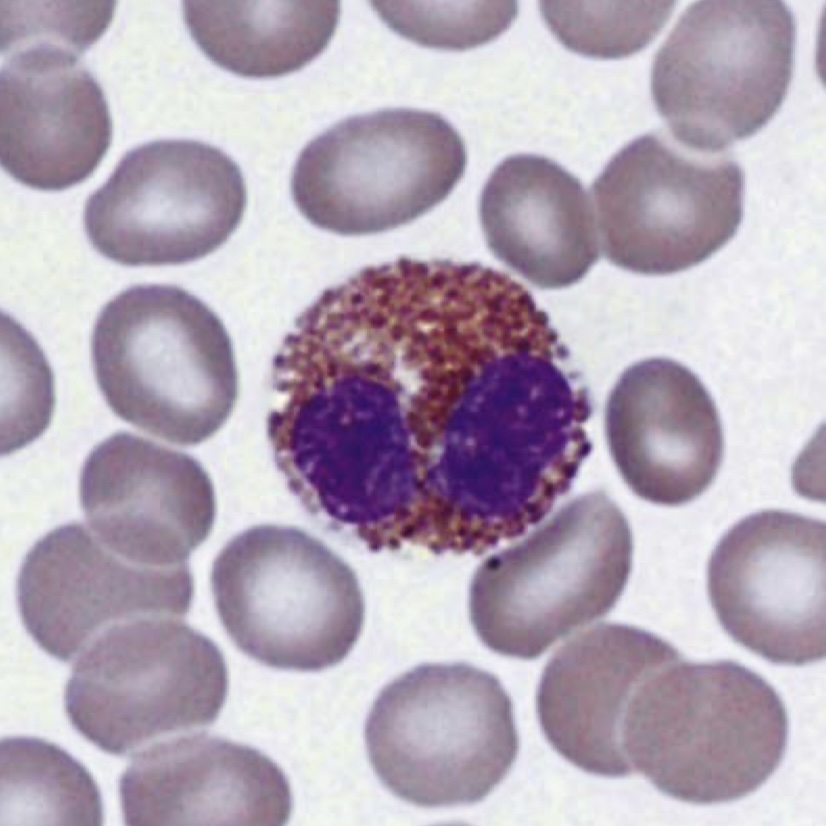
ائوزینوفیلها معمولاً از نوتروفیلها بزرگترند و هسته آنها معمولاً دو لوب دارد (گاهی یک یا سه لوب نیز مشاهده میشود).
گرانولهای اختصاصی ائوزینوفیل در مرحله میلوسیت ائوزینوفیل ظاهر میشوند و از همین مرحله است که پیشسازهای ائوزینوفیل زیر میکروسکوپ قابل تشخیص میشوند. این گرانولها در ابتدا فاقد کریستالوئید هستند، اما با بلوغ سلول به تدریج حاوی کریستالوئید شده و رنگ آنها از سبز زیتونی به نارنجی یا آجری (در رنگآمیزی رایت-گیمسا) تغییر میکند. این رنگ نارنجی به دلیل واکنش پروتئین بازی اصلی (MBP) با رنگ ائوزین است.
گرانولهای ائوزینوفیل را میتوان به چهار گروه اصلی طبقهبندی کرد:
- گرانولهای اولیه: حاوی کریستالهای شارکوت-لیدن هستند. این کریستالهای 6 وجهی از آنزیم لیزوفسفولیپاز مشتق میشوند و در افراد مبتلا به آسم، آلرژی و واکنشهای التهابی مزمن مشاهده میشوند.
- گرانولهای اختصاصی بزرگ: حاوی پروتئینهایی نظیر پروتئین بازی اصلی (MBP)، پروتئین کاتیونی ائوزینوفیلی (ECP) و نوروتوکسین مشتق از ائوزینوفیل (EDN) میباشند.مهم ترین این پروتئین ها، MBP است که برای انگلها و سلولهای بدن سمی است، هپارین را خنثی میکند و باعث رها شدن هیستامین از بازوفیلها میشود.
- گرانولهای اختصاصی کوچک: حاوی آنزیمهایی مانند آریل سولفاتاز، پراکسیداز و اسید فسفاتاز هستند.
کینتیک ائوزینوفیلها: از مغز استخوان تا بافتها
کنتیک ائوزینوفیلها شبیه به نوتروفیلهاست. پس از بلوغ، ائوزینوفیلها برای چند روز در مغز استخوان ذخیره میشوند و سپس وارد دو حوضچه گرانولوسیتی در گردش (CGP) و گرانولوسیتی حاشیهای (MGP) در خون میشوند.
نیمهعمر ائوزینوفیلها در خون 13 تا 18 ساعت است، اما پس از ورود به بافتها، حداقل 6 روز در آنجا زنده میمانند. نکته قابل توجه این است که تعداد ائوزینوفیلها در بافتها حداقل 100 برابر بیشتر از خون است، که نشاندهنده نقش اصلی آنها در پاسخهای ایمنی موضعی است.
عملکرد ائوزینوفیلها: دفاع در برابر انگل و تنظیم آلرژی
ائوزینوفیلها سلولهای تخصصی در مقابله با عفونتهای انگلی هستند. عملکرد اصلی آنها شامل:
- دفاع ضد میکروبی: آنها توانایی فاگوسیتوز ذرات خارجی پوشیده شده با IgG را دارند، اما تخصص اصلی آنها در مبارزه با انگلهاست.
- تعدیل واکنشهای آلرژیک و التهابی: ائوزینوفیلها نقش دوگانهای در واکنشهای آلرژیک ایفا میکنند؛ هم میتوانند در تشدید پاسخهای حساسیت نقش داشته باشند و هم در تعدیل و کنترل آنها.
- شرکت در پاتوژنز آسم: تجمع و فعالیت بیش از حد ائوزینوفیلها در مجاری تنفسی میتواند به التهاب و آسیب بافتی در بیماری آسم منجر شود.
تولید، تکامل و عملکرد مونوسیت/ماکروفاژ
تکامل ردهی مونوسیتی
مرحلهی پروژنیتوری تمایز ردهی مونوسیت به شکل زیر است؛
سلول بنیادی خونساز ← CFU-GEMM ← CFU-GM ← CFU-M
(M-CSF) CSF-1، منجر به افزایش تمایز CFU- GM به مونوسیت می شود.
تمایز پره کورسوریِ ردهی مونوسیت به شرح زیر میباشد:
مونوبلاست ← پرومونوسیت ← مونوسیت ← ماکروفاژ
زودرسترین سلول قابل تشخیص ردهی مونوسیتی، پرومونوسیت است و تا حدی از میلوبلاست بزرگتر است و هستهی آن بیضی یا دندانهدار با الگوی کروماتین ظریف و یکنواخت است.
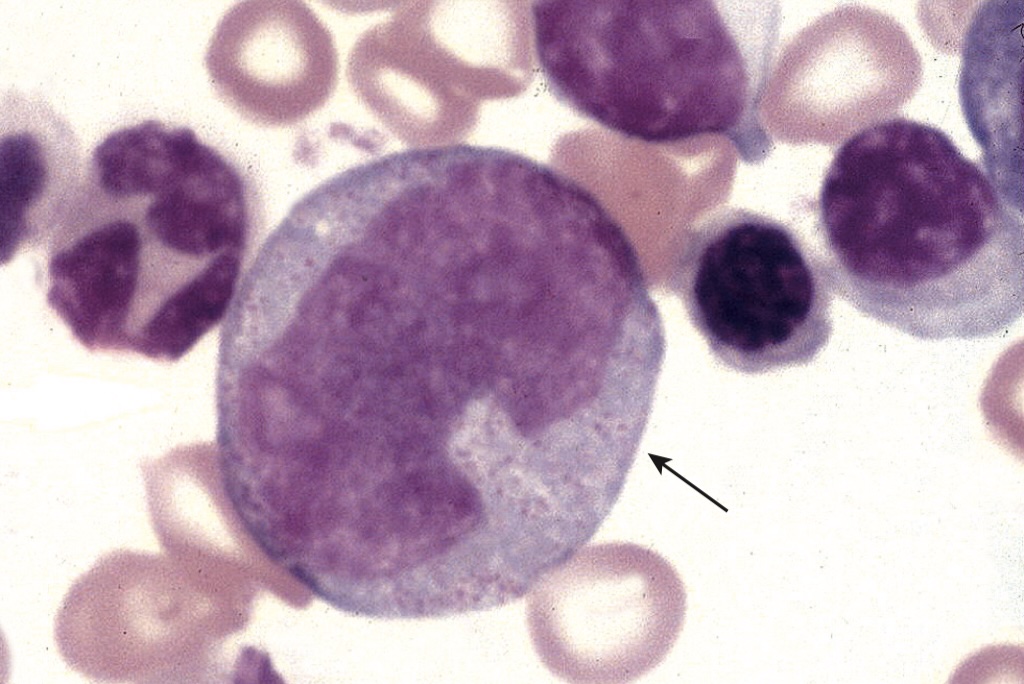
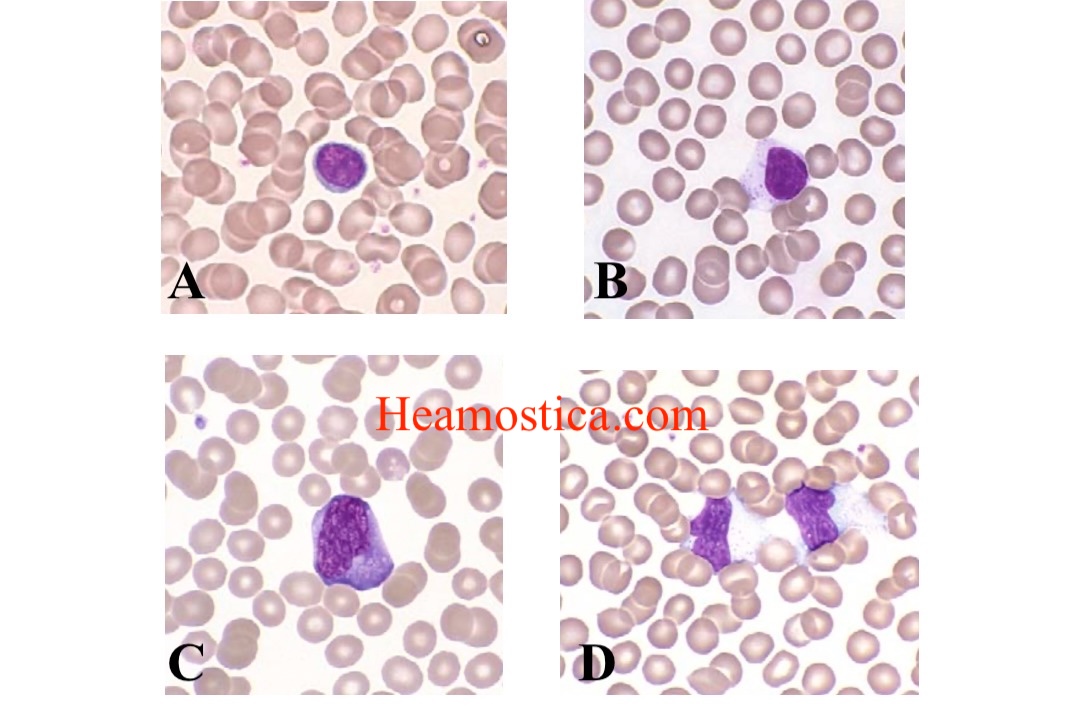
مونوسیت بزرگترین سلول طبیعی خون است و قطری حدود دو تا سه برابر اریتروسیت دارد. در شکل ۳-۱۷ تصویر مونوسیت مشاهده می کنید.
مونوسیتها پس از ورود به بافت به ماکروفاژ تبدیل میشوند. ماکروفاژها کمی بزرگتر از مونوسیتها میباشند و پای کاذب دارند. اگرچه ماکروفاژها در همهی بافتهای بدن حضور دارند، ولی بیشترین تعداد آنها در کبد، طحال، BM و روده وجود دارند. به مجموعهی ماکروفاژهای موجود در کبد و طحال سیستم رتیکلواندوتلیال میگویند.
بر اساس محل حضور ماکروفاژ در بافتهای مختلف، نامهای مختلفی میگیرند؛ به گونهای که در کبد، سلولهای کوپفر، در بافت همبند، هیستوسیت، در پوست هیستوسیت یا سلول های لانگرهانس، در استخوان استئوکلاست و در جزایر اریتروبلاستیک سلولهای پرستار نامیده می شوند.
ماکروفاژها در عفونتهای فعال به صورت واکوئوله، بزرگ و چند هستهای و مملو از عوامل فاگوسیته شده دیده میشوند که در کل به فرمهای ارتشاحی آنها هیستوسیت میگویند. افزایش تعداد هیستوسیتها را هیستوسیتوز میگویند که میتواند به دو فرم خوشخیم و بدخیم رخ دهد.
مونوسیتها CD11, CD14, CD4, CD64 را بیان میکنند.
CD4 که علاوه بر سلولهای Th در مونوسیت و ماکروفاژ هم بیان میشوند گیرندهی HIV است. به همین دلیل تعداد مونوسیتها در عفونت HIV کاهش مییابد.
توزیع و کنتیک مونوسیت/ماکروفاژ
پس از شکلگیری پرومونوسیت، این سلولها تحت تأثیر M-CSF قرار گرفته و در مدت زمانی حدود ۶۰-۵۰ ساعت، ۲ یا ۳ تقسیم میتوز انجام داده و به مونوسیت تبدیل شده و وارد خون میشوند. مونوسیتها نیز مثل گرانولوسیتها دارای حوضچههای در گردش (CMP) و حوضچهی حاشیهای (MMP) هستند. نسبت مونوسیتهای حاشیهای به مونوسیتهای در گردش برابر ۵/۳ به ۱ است یعنی تعداد مونوسیتهای در حاشیهی عروق ۵/۳ برابر مونوسیتهای در گردش است.
مونوسیتها بعد از ورود به خون حدود ۵/۸ ساعت در خون حضور دارند سپس به بافتها مهاجرت کرده و به ماکروفاژ تمایز مییابند. این زمان (۵/۸ ساعت) در بیماران مبتلا به اسپلنومگالی و عفونت حاد کوتاه میشود و در مونوسیتوز، افزایش مییابد.
مشاهدهی فاگوسیتوز در مونوسیتها یا حضور ماکروفاژها در گسترهی خون محیطی حالت پاتولوژیک محسوب میشود و اغلب حاکی از وجود یک عفونت فعال است.
به طور کلی، ماکروفاژ، ماستسل و پلاسما سلها به طور طبیعی در خون وجود ندارند و حضور آنها در خون محیطی به احتمال زیاد نشان دهندهی وجود اختلال یا بیماری است.
عملکرد ماکروفاژها
در واقع ماکروفاژها سلولهای عملکردی ردهی مونوسیتی میباشند. عملکردهای ماکروفاژ به شرح زیر میباشند:
- فاگوسیتوز باکتریها و سایر عوامل عفونی و بقایای سلولی و سلولهای فرسوده: ماکروفاژها قویترین فاگوسیتهای بدن هستند و قادرند باکتریها، قارچها، تک یاختهها و ویروسها و سلول های آسیب دیده را فاگوسیتوز کنند. ماکروفاژها (سلولهای پرستار) در خارج شدن هسته اورتوکروماتیک نورموبلاست و تولید رتیکلوسیت نقش مهمی دارند. در بیماری لوپوس اریتروماتوز سیستمیک (SLE) ماکروفاژها و نوتروفیل ها، هستههای هموژن ناشی از بیماری را فاگوسیتوز میکنند که در این حالت به آن سلول (LE cell) LE میگویند. البته قابل ذکر است که سلول LE عمدتاً نوتروفیل میباشد.
- عرضهی آنتیژن به سلول T: ماکروفاژها دارای HLA کلاس I و II هستند و به عنوان گروهی از APCهای حرفهای عمل کرده و آنتیژنها را جهت فعال شدن سلول T به این سلولها عرضه میکنند در نتیجه ماکروفاژها جزء مهمی از هر دو ایمنی ذاتی و اکتسابی هستند.
- شرکت در متابولیسم آهن؛ ماکروفاژها میتوانند در BM، آهن را در قالب فریتین ذخیره کنند.
- شرکت در سایتوتوکسیسیته وابسته به آنتیبادی (ADCC)
- تولید و ترشح مواد فعال بیولوژیک مثل سیتوکاینها، اجزای کمپلان، فاکتورهای رشد و فاکتورهای رگزایی.
تولید، تمایز و عملکرد بازوفیل ها و ماست سل ها
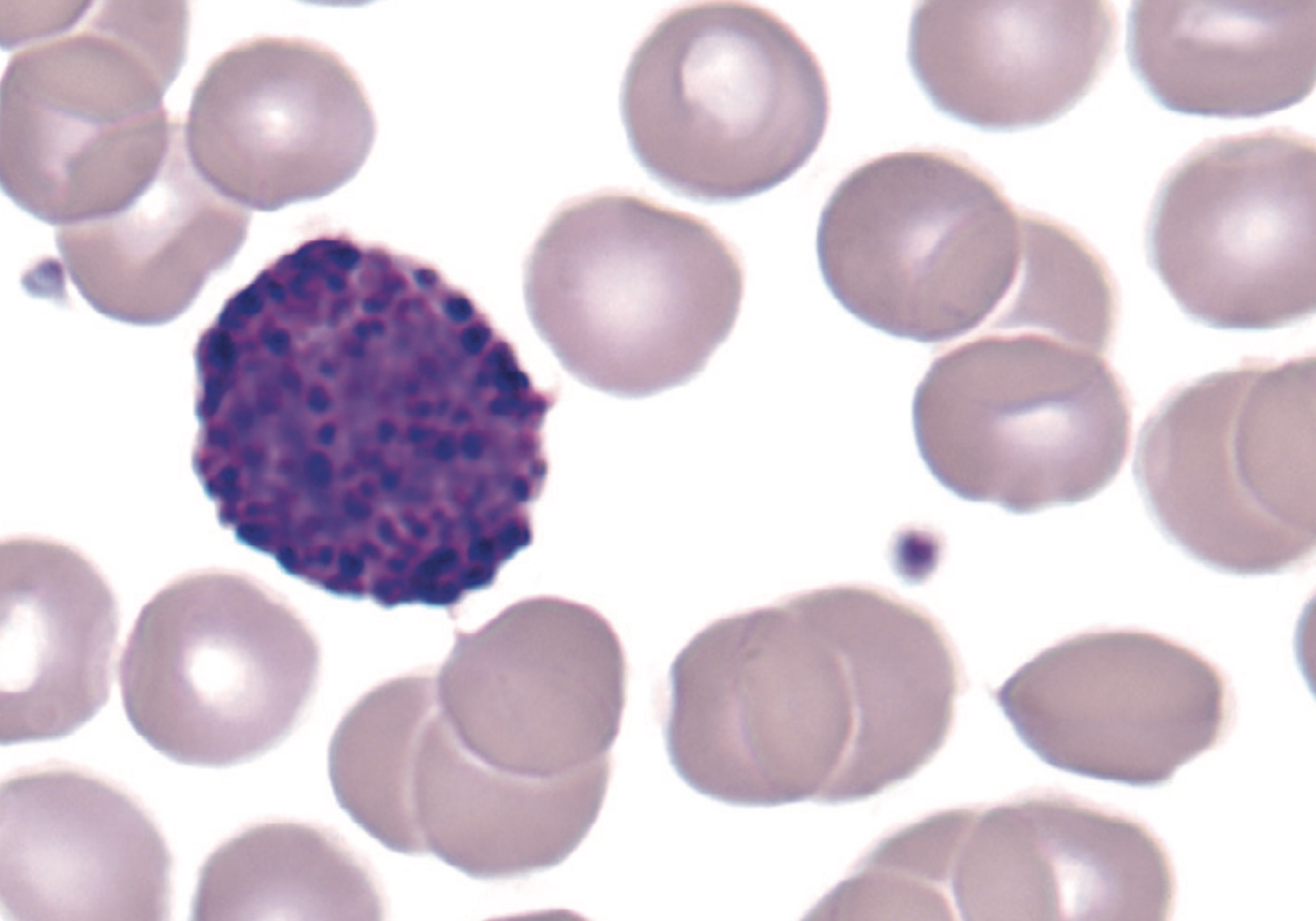
بازوفیل ها و ماستسل ها دو دسته از سلول های خونی با شباهت های مورفولوژیک و عملکردی هستند. با اینحال میتوان بازوفیل ها را لکوسیت های واقعی در نطر گرفت زیرا در مغز استخوان تولید می شوند و در جریان خون گردش میکنند اما ماستسل ها در بافت ها سکونت دارند و هنوز به طور قطعی منشاء این سلول ها مشخص نیست و اکثر مطالعات، منشاء آن ها را سلول های بنیادی مزانشیمی –و نه سلول های بنیادی خونساز- میدانند. بازوفیل ها کمترین تعداد سلول های خون محیطی را تشکیل میدهند.
IL-3 مهم ترین فاکتور رشد برای بازوفیل هاست در حالیکه c-kit ligand تولید و فعالیت ماست سل ها را افزایش میدهد.
بازوفیل بالغ دارای هسته ی دو لوبه است که معمولا به طور کامل توسط گرانول ها پوشانده شده است. سیتوپلاسم بی رنگ است و حاوی تعداد زیادی گرانول های آبی- مشکی است . گرانولهای بازوفیل به شدت اسیدی میباشند و تمایل بالایی به رنگهای قلیایی (مثل آزور B) دارند. گرانولهای اختصاصی بازوفیلها حاوی هپارین، هیستامین هستند.
ماستسلها به طور گستردهای در بافتهای مختلف مثل روده، مجاری ادراری تناسلی، ریه، BM، تیموس و طحال قرار دارند و برخلاف بازوفیلها، ماستسلها سلول نهایی نبوده و قادرند مجدداً در بافتها تکثیر یابند.
بازوفیلها و ماستسلها در واکنشهای ازدیاد حساسیت فوری و برخی واکنشهای ازدیاد حساسیت تأخیری نقش دارند؛ IgE به مولکول (FCɛR) CD23 در سطح بازوفیلها و ماستسلها متصل شده و منجر به دگرانولاسیون و آزاد شدن واسطههای ازدیاد حساسیت فوری (مثل هیستامین، هپارین، ECFA و SRSA) میشود. به استثناء حضور آنزیمهای پروتئولیتیک و سروتونین در ماستسلها و فقدان آن در بازوفیل، این دو نوع سلول خصوصیات بیوشیمیایی مشابهی دارند.
تولید، تمایز و عملکرد پلاکتها
پلاکت ها از سلول های پلی پلوئید[1] به نام مگاکاریوسیت در مغز استخوان تولید می شوند. مهم ترین فاکتور رشد جهت تولید مگاکاریوسیت ها و پلاکت ها ترومبوپوئتین است.
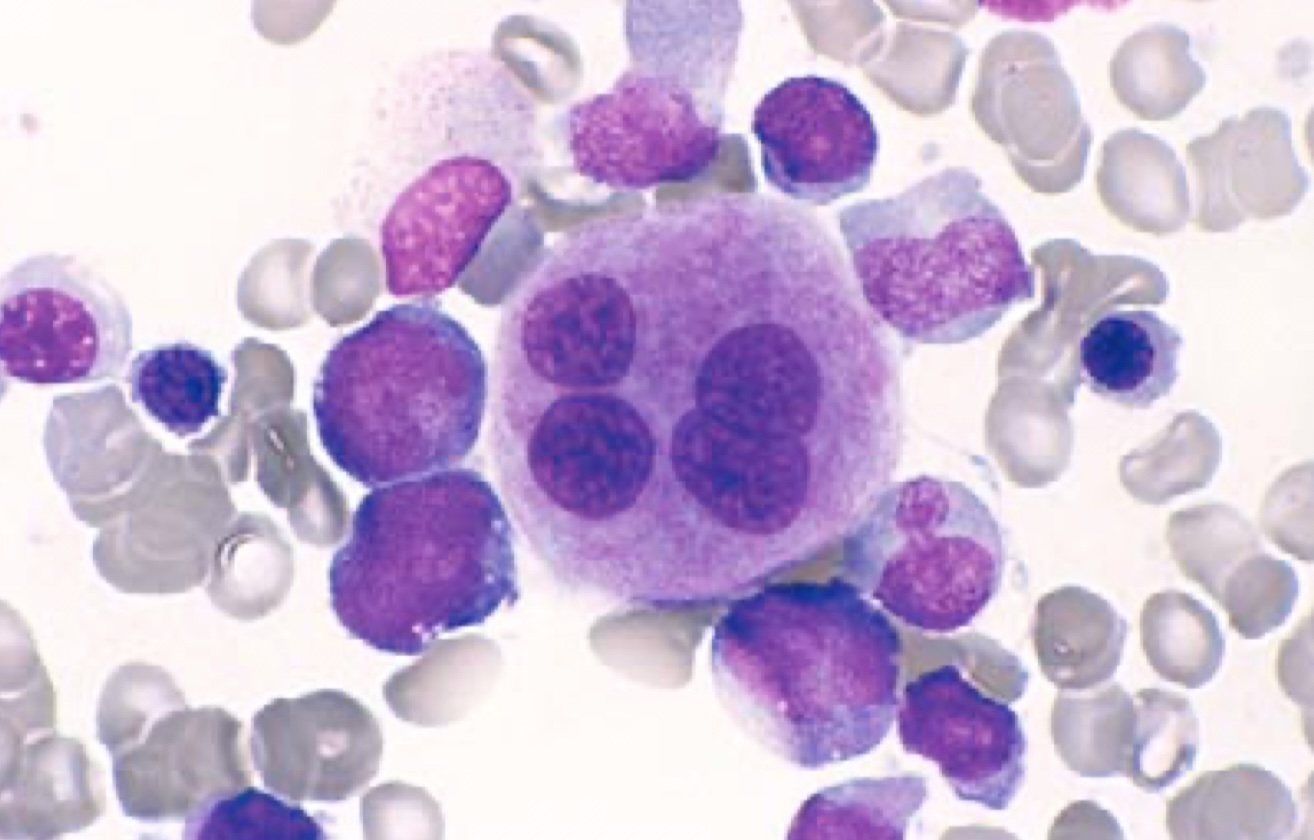
مگاکاریوسیتها بزرگترین سلولهای خونساز مغز استخوان هستند. هستهی مگاکاریوسیت بسیار لوبوله و فاقد هستک است .
مگاکاریوسیتها کمتر از ۱ درصد سلولهای هستهدار BM را تشکیل میدهند و در لام با عدسی ۱۰ باید ۳-۱ مگاکاریوسیت مشاهده شود.
نکته: مگاکاریوسیت مارکرهای CD42, CD61, CD41 را بیان میکنند.
مگاکاریوسیت ممکن است به صورت نادر در لام خون محیطی مشاهده شود. در MPN, MDS، اختلالات میلوفیتزیک و AML-M7 ممکن است تعداد مگاکاریوسیت در خون محیطی افزایش پیدا کند.
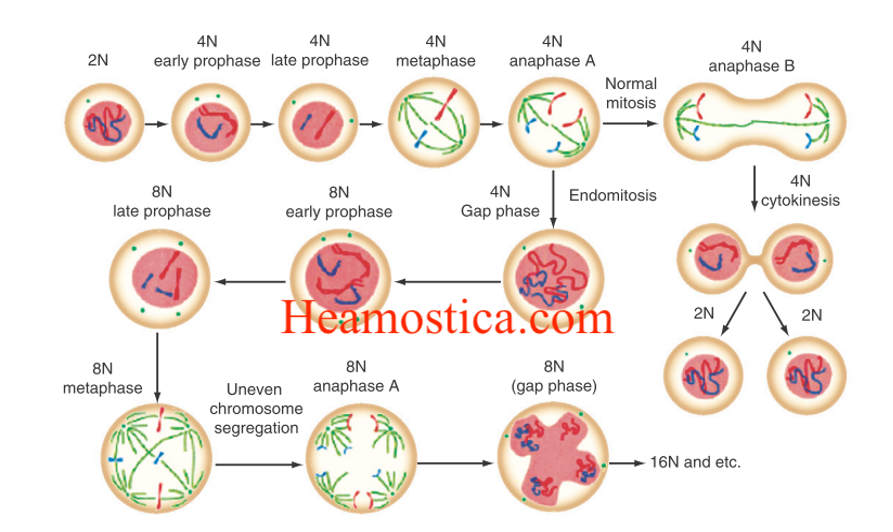
تکامل مگاکاریوسیت به صورت اندومیتوز است و به این معناست که هسته تقسیم میشود ولی سیتوپلاسم تقسیم نمیشود و به عبارت دیگر مراحل پروفاز، متافاز و آنافاز A انجام میشود ولی آنافاز B، تلوفاز و سیتوکینز انجام نمیشود در شکل زیر تفاوت میتوز معمولی و اندومیتوز را مشاهده میکنید.
همانگونه که از شکل مشخص است، اندومیتوز باعث تولید سلولهای با پلوئیدی مختلف از 8n تا 128 n میشود.
اولین مرحلهای که مگاکاریوسیت قادر به تولید پلاکت است مرحله 8n است.
به طور متوسط از هر مگاکاریوسیت ۲۰۰۰ تا ۵۰۰۰ پلاکت تولید میشود.
پلاکتهای رتیکوله (Reticulated platelet): پلاکتهای تازه تولید شدهای میباشند که دارای بقایای RNA هستند و علامتِ ترومبوپوئز مؤثر میباشند. پلاکتهای رتیکوله، بزرگتر، مؤثرتر و فعالتر از پلاکت معمولی هستند.
در گسترشهای خونی با رنگآمیزی رایت، پلاکتها گرد و بیضی بوده و دارای قطر 2-4 میباشند . به طور متوسط به ازای هر ۱۰ تا ۳۰ اریتروسیت، یک پلاکت مشاهده میشود. در بزرگنمایی 1000× در هر فیلد، 20-7 پلاکت مشاهده میشود. برای تخمین تعداد پلاکتها از روی لام، تعداد پلاکتهای شمارش شده در هر فیلد 1000× را در عدد 15000 ضرب میکنیم مثلاً اگر 10 پلاکت مشاهده شود، شمارش تخمینی پلاکت ۱۵۰۰۰۰ در میکرولیتر است.
پلاکتهای غولآسا یا بزرگ در سندروم برنارد- سولیر، سندرومهای میلومتیزیک و MPNها افزایش مییابد.
در هر زمان حدود یک سوم پلاکتها در گردش خون قرار دارد و دو سوم آنها در طحال ذخیره میشوند در نتیجه در افرادی که اسپلنکتومی شدهاند همهی پلاکتها وارد خون شده و ترومبوسیتوز رخ میدهد. در مقابل در افرادی که به اسپلنومگالی مبتلا هستند حدود ۸۰ تا ۹۰ درصد پلاکتها در طحال وجود دارند (محبوس میشوند) و در نتیجه ترومبوسایتوپنی مشاهده میشود.
طول عمر پلاکتها در گردش خون ۱۱-۸ روز است.
تعداد پلاکتها دارای تغییرات شبانهروزی است و در صبح کاهش و در عصر افزایش مییابد.
عملکرد پلاکتها
اولین و مهمترین نقش آنها در توقف خونریزی (هموستاز) است. هنگامی که رگ خونی آسیب میبیند، پلاکتها به محل آسیب چسبیده، فعال میشوند و با تجمع در کنار یکدیگر یک پلاگ پلاکتی موقت تشکیل میدهند. این پلاگ پلاکتی با فعال کردن آبشار انعقادی و تشکیل رشتههای فیبرین، به یک لخته خونی پایدار تبدیل میشود. علاوه بر این، پلاکتها با ترشح فاکتورهای رشد مختلف، به ترمیم بافتهای آسیبدیده و رگزایی (تشکیل عروق خونی جدید) در محل زخم کمک میکنند و به این ترتیب در فرآیند بهبودی نقش مؤثری دارند.
- polyploid
تولید، تمایز و عملکرد لنفوسیتها
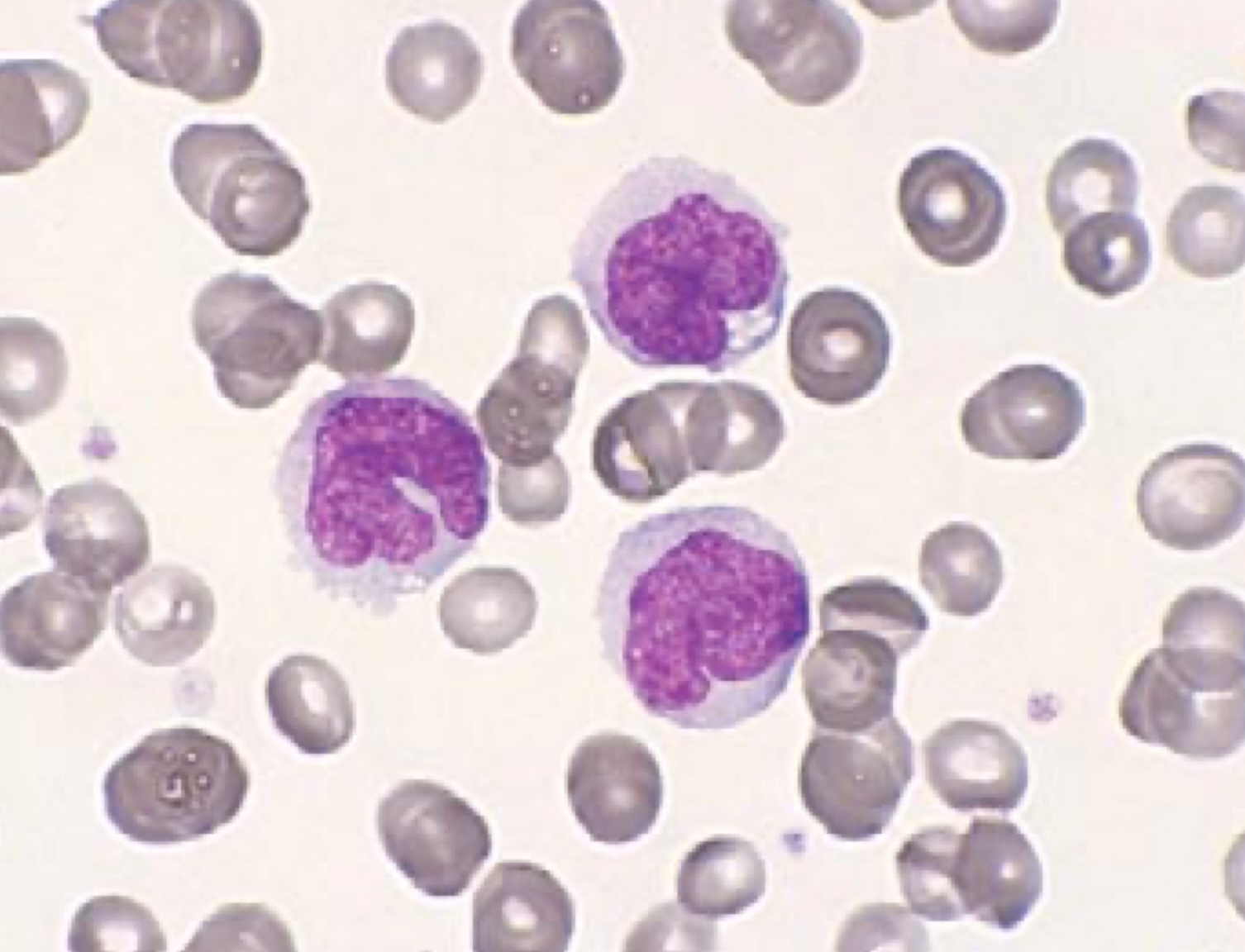
لنفوسیت های B و T دستهای از لکوسیت ها هستند که سیستم ایمنی تطبیقی انسان را تشکیل میدهند. گیرنده های لنفوسیت های B و T باید تنوع بسیار بالایی داشته باشد تا بتواند انواع آنتی ژن ها را شناسایی کند. تنوع گیرنده های آنتی ژنی سلول های B و T به فرایندی به نام بازآرایی ژنی[2] بستگی دارد. ژن هایی که گیرنده های سلول های B و T یعنی BCR و TCR را کد میکنند از طریق بازآرایی قطعات ژنی نواحی V ، D و J میتوانند تعداد بیشماری BCR و TCR اختصاصی علیه آنتی ژن های مختلف تولید کنند. در شکل زیر تصویر لنفوسیت را در خون محیطی مشاهده میکنید.
تولید و تمایز سلول های B
تکثیر پروژنیتور های سلول B به پیامرسانی IL-7 ( و گیرنده اش IL-7 R ) و مسیر پیامرسانی JAK-STAT وابسته است.
اولین پیشساز متعهد به رده ی سلولی لنفوسیت B، در مغز استخوان، Pro B Cell است که ایمونوگلوبولین تولید نمیکند ولی به واسطه ی بیان CD10، CD19 و tdt میتوان آنها را تشخیص داد. این سلول فاقد ایمونوگلوبولین (Ig) سطحی یا سیتوپلاسمی است.
هنگامی که یک بازآرایی مؤثر زنجیره ی سنگین IgM ( یعنی µ) رخ دهد سلول به Pre B Cell تبدیل میشود.
در مرحله ی بعد تکامل هر سلول B یک زنجیره ی سبک k را بازآرایی میکنند که با اتصال به زنجیره ی µ از پیش ساخته، یک IgM کامل را در سطح سلول بیان میکند که به این سلول، سلول B نابالغ[3] میگویند.
بیان IgD بر سطح سلول باعث تبدیل شدن سلول B نابالغ به سلول B بالغ[4] میشود. به عبارت دیگر سلول B بالغ، IgM+، IgD+ است.
در نهایت تعدادی از سلول های B با میل پیوندی بالا انتخاب میشوند، تکثیر میشوند و به سلول های B خاطره یا پلاسما سل های مترشحه ی آنتی بادی تمایز مییابند. تمایز سلول های B به پلاسما سل های مترشحه ی آنتی بادی، شامل تغییرات ساختمانی عمده به خصوص در اجزای شبکه آندوپلاسمی و مسیر ترشحی و همچنین افزایش تولید ایمونوگلوبولین است.
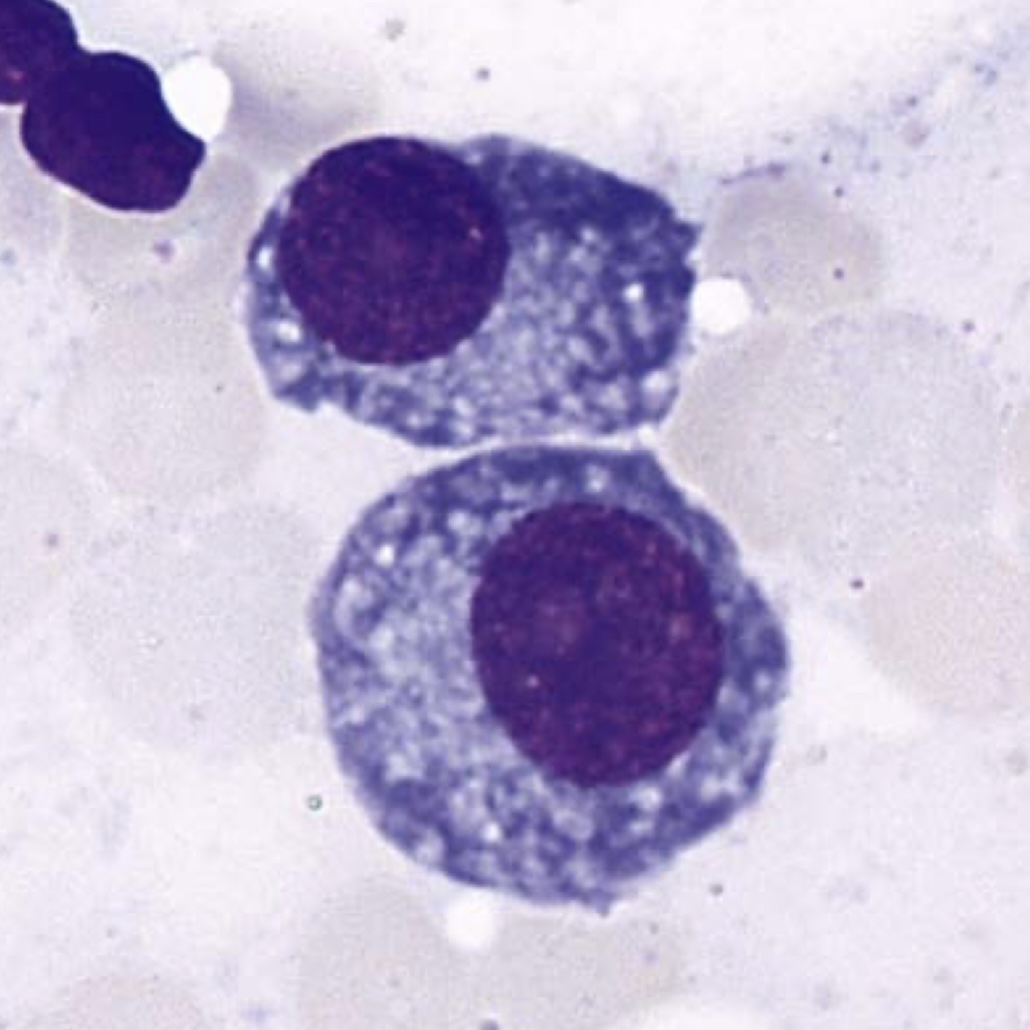
پلاسما سل ها، CD38 و CD138 را بیان میکنند. پلاسما سل ها دارای سیتوپلاسم آبی گسترده هستند که معمولا حاوی واکوئول هم هست. پلاسما سل ها دارای هستهی گرد غیر مرکزی[5] است و یک هاله ی سفید که دستگاه گلژی است در مجاورت هسته مشاهده میشود .
تولید و تمایز سلول های T
بلوغ لنفوسیت های T از پیشساز های متعهد شامل مراحل متوالی بازآرایی و بیان ژن های TCR، تکثیر سلولی، گزینش القا شده توسط آنتی ژن و تعهد به تولید زیرمجموعه های با فنوتیپ و عملکرد مجزا است.
ریز محیط تیموس برای تمایز و بلوغ سلول های T ضروری است، در نتیجه لنفوسیت های T مشتق از پیشساز های کبد جنینی و مغز استخوان افراد بالغ، به تیموس مهاجرت کرده و بقیه ی مسیر تکامل را در آنجا طی میکند. سلول های T به واسطه ی بیان گیرنده ی کموکاین CCR9 که به کموکاین CCL25 که در تیموس بیان میشود متصل شده و به قشر تیموس وارد میشود. مراحل تکامل سلول های T به شرح زیر است:
- تیموسیت های منفی مضاعف[6]: سلول های T هستند که به تازگی از مغز استخوان به تیموس رسیدهاند و ژن TCR را در حالت پایه دارند ولی TCR، CD3، CD4 و CD8 را بیان نمیکنند.
- Pre T Cells: مرحله ای است که سلول، ژن TCR β را به صورت VDJ بازآرایی میکند و آن را به همراه یک پروتئین به نام Pre-Tα در سطح سلول بیان میکند.
- تیموسیت های مثبت مضاعف[7]: در این مرحله هر دو مولکول CD4 و CD8 در سطح سلول بیان میشوند. به علاوه زنجیره ی TCR α نیز بیان میشود که با TCR β ترکیب شده و TCR αβ را در سطح سلول به وجود میآورد. ۹۰ درصد سلول های T، TCR αβ و ۱۰ درصد TCR γδ را بیان میکنند. باید توجه کرد که برای بیان کمپلکس TCR در سطح سلولهای T باید همه ی اجزای آن یعنی CD3، ζ و در زنجیره ی TCR به طور همزمان وجود داشته باشند.
- سلول های T مثبت منفرد[8]: در نهایت بیان یکی از مارکر های CD4 یا CD8 سرکوب میشود و سلول های T به سلولهای T CD4-CD8+ ( سلول های T سایتوتوکسیک) و یا سلول های T CD4+ CD8- ( سلول های T کمکی) تبدیل میشوند. سلول های T سایتوتوکسیک مستقیما سلول های بیگانه را میکشند ولی سلول های T کمکی باعث فعال شدن لنفوسیت های B میشوند.
- Gene Rearrangement
- Immature B Cell
- Mature B Cells
- Eccentric
- Double-Negative Thymocytes
- Double-Positive Thymocytes
- Single-Positive T cells
سوالات چهار گزینهای
- کدام یک از فاکتورهای رشد زیر، مهمترین نقش را در تمایز نوتروفیلها ایفا میکند؟
- GM-CSF
- IL-3
- G-CSF
- IL-5
- کدام مرحله از تمایز نوتروفیلها، آخرین مرحلهای است که سلول توانایی تقسیم میتوز دارد؟
- میلوبلاست
- پرومیلوسیت
- میلوسیت
- متامیلوسیت
- کدام یک از موارد زیر، نشانهای از “شیفت به چپ نوتروفیلی” است؟
- افزایش تعداد نوتروفیلهای بالغ با هستههای 5 لوبه یا بیشتر.
- کاهش تعداد باند سلها در خون محیطی.
- ورود باند سل و گاهی میلوسیتها به خون محیطی.
- افزایش نیمهعمر نوتروفیلها در خون.
- کدام پروتئین در گرانولهای اختصاصی بزرگ ائوزینوفیلها وجود دارد و برای انگلها سمی است؟
- لیزوزیم
- لاکتوفرین
- میلوپراکسیداز
- پروتئین بازی اصلی (MBP)
- نیمهعمر ائوزینوفیلها در خون محیطی چقدر است؟
- 2 تا 5 روز
- 6.5 تا 9 ساعت
- 13 تا 18 ساعت
- 6 روز
- کدام سلول زیر به عنوان قویترین فاگوسیتهای بدن شناخته میشود؟
- نوتروفیل
- ائوزینوفیل
- ماکروفاژ
- لنفوسیت
- کدام مارکر بر روی سطح مونوسیتها و ماکروفاژها بیان میشود و گیرندهی HIV است؟
- CD11
- CD14
- CD64
- CD4
- کدام فاکتور رشد، مهمترین نقش را در تولید و فعالیت ماست سلها دارد؟
- IL-3
- IL-5
- G-CSF
- c-kit ligand
- فرآیند تولید پلاکتها از مگاکاریوسیتها در مغز استخوان به چه نامی شناخته میشود؟
- میتوز
- اندومیتوز
- میوز
- گرانولوپوئز
- کدام مارکرهای سطحی برای تشخیص سلولهای B پروژنیتور (Pro B Cell) استفاده میشوند؟
- CD3, CD4, CD8
- CD13/33, CD34, CD15/117
- CD10, CD19, tdt
- CD38, CD138
کلید سوالات چهار گزینهای
- ج
- ج
- ج
- د
- ج
- ج
- د
- د
- ب
- ج
۱۰ سوال رایج با جواب
- گلبول های سفید (لکوسیتها) چه نقشی در بدن ایفا میکنند؟پاسخ: گلبول های سفید سربازان خط مقدم بدن هستند که با شناسایی و نابودی عوامل بیماریزا نظیر باکتریها، ویروسها، قارچها و سلولهای سرطانی، بدن را در برابر عفونتها و بیماریها محافظت میکنند.
- فرآیند تولید گلبول های سفید در کجا صورت میگیرد؟پاسخ: فرآیند تولید گلبول های سفید (هماتوپوئیز) از سلولهای بنیادی خونساز در مغز استخوان آغاز میشود.
- مهمترین فاکتور رشد برای تمایز نوتروفیلها چیست؟پاسخ: G-CSF (Granulocyte Colony-Stimulating Factor) مهمترین فاکتور رشد در تمایز نوتروفیلها است.
- منظور از “شیفت به چپ نوتروفیلی” چیست و چه اهمیتی دارد؟پاسخ: “شیفت به چپ نوتروفیلی” یا باندمی به وضعیتی گفته میشود که در آن باند سلها و گاهی میلوسیتها (اشکال نارس نوتروفیل) به دلیل افزایش نیاز بدن به نوتروفیل، وارد خون محیطی میشوند. این وضعیت معمولاً نشانهای از عفونت یا التهاب شدید است.
- گرانولهای اختصاصی ائوزینوفیلها حاوی چه پروتئینهایی هستند و رنگ نارنجی آنها به چه دلیلی است؟پاسخ: گرانولهای اختصاصی ائوزینوفیلها حاوی پروتئینهایی نظیر پروتئین بازی اصلی (MBP)، پروتئین کاتیونی ائوزینوفیلی (ECP) و نوروتوکسین مشتق از ائوزینوفیل (EDN) میباشند. رنگ نارنجی آنها به دلیل واکنش پروتئین بازی اصلی (MBP) با رنگ ائوزین در رنگآمیزی رایت-گیمسا است.
- نقش اصلی ائوزینوفیلها در سیستم ایمنی بدن چیست؟پاسخ: ائوزینوفیلها سلولهای تخصصی در مقابله با عفونتهای انگلی و همچنین تعدیل واکنشهای آلرژیک و التهابی هستند.
- چرا تعداد ائوزینوفیلها در بافتها بسیار بیشتر از خون است؟پاسخ: تعداد ائوزینوفیلها در بافتها حداقل 100 برابر بیشتر از خون است، که نشاندهنده نقش اصلی آنها در پاسخهای ایمنی موضعی در بافتها و نه صرفاً در جریان خون است.
- ماکروفاژها چه نامهای دیگری در بافتهای مختلف بدن میگیرند؟پاسخ: ماکروفاژها بر اساس محل حضورشان در بافتهای مختلف نامهای متفاوتی دارند، از جمله: سلولهای کوپفر در کبد، هیستوسیتها در بافت همبند و پوست (یا سلولهای لانگرهانس در پوست)، استئوکلاستها در استخوان و سلولهای پرستار در جزایر اریتروبلاستیک.
- منظور از “پلاکتهای رتیکوله” چیست و چه اهمیتی دارند؟پاسخ: پلاکتهای رتیکوله، پلاکتهای تازه تولید شدهای هستند که دارای بقایای RNA میباشند. حضور آنها نشانهی ترومبوپوئز مؤثر است و این پلاکتها معمولاً بزرگتر، مؤثرتر و فعالتر از پلاکتهای معمولی هستند.
- چرا در بیماران مبتلا به اسپلنکتومی (برداشتن طحال) ترومبوسیتوز (افزایش پلاکت) رخ میدهد؟پاسخ: به طور طبیعی، حدود یک سوم پلاکتها در گردش خون هستند و دو سوم آنها در طحال ذخیره میشوند. در افرادی که طحال آنها برداشته شده، این محل ذخیره از بین میرود و تمام پلاکتها وارد جریان خون میشوند که منجر به افزایش تعداد پلاکتها یا ترومبوسیتوز میگردد.
جهت مطالعه بیشتر به لینک زیر مراجعه کنید: