تفاوت تست رایت و ویدال (Wright vs Widal Test)
خلاصه: تفاوت تست رایت و ویدال در عامل بیماریزا، نوع آنتیژن، تفسیر تیتر و کاربرد بالینی است. رایت برای بروسلوز (Brucellosis) با آنتیژن بروسلا و انکوباسیون ۲۴ ساعته انجام میشود؛ ویدال برای تیفوئید با آنتیژنهای O و H سالمونلا و معمولاً ۲ ساعته است. رعایت کنترل کیفی، محدودههای تیتر و اپیدمیولوژی منطقه در تفسیر نتایج حیاتی است.
جهت عضویت در کانال آموزشی در تلگرام به لینک زیر مراجعه کنید:
https://t.me/hematology_education
فهرست مطالب
مقدمه
در علوم آزمایشگاهی، دو تست سرولوژیک پرکاربرد برای تشخیص بیماریهای باکتریایی، تست رایت (Wright) و تست ویدال (Widal) هستند. با اینکه هر دو تست بر پایهٔ واکنش آنتیژن–آنتیبادی و پدیدهٔ آگلوتیناسیون طراحی شدهاند، اما از نظر عامل بیماری، نوع آنتیژن، تفسیر نتایج و کاربرد بالینی تفاوتهای مهمی دارند. در این مقاله به بررسی کامل و علمی تفاوت تست رایت و ویدال پرداختهایم.
تعریف هر تست
🧫 تست رایت (Wright Test)
تست رایت، یا Wright agglutination test، آزمایشی است برای تشخیص بروسلوز (تب مالت) که عامل آن باکتریهای Brucella abortus و Brucella melitensis هستند.
در این تست، سرم بیمار با آنتیژن کشتهٔ بروسلا ترکیب میشود و در صورت وجود آنتیبادی اختصاصی (IgM یا IgG)، واکنش آگلوتیناسیون مشاهده میشود.
🔍 تست رایت یک آزمایش نیمهکمی و لولهای (Tube Agglutination) است.
جهت مطالعه ی جانع در مورد روش انجام آزمایش رایت به لینک زیر مراجعه کنید:
روش انجام آزمایش رایت لوله ای: راهنمای جامع برای تشخیص بروسلوز
🧫 تست ویدال (Widal Test)
تست ویدال یک آزمایش آگلوتیناسیون لولهای است که برای تشخیص تب تیفوئید (Typhoid Fever) ناشی از باکتری Salmonella typhi و گاهی S. paratyphi A و B استفاده میشود.
در این تست از دو نوع آنتیژن استفاده میشود:
- آنتیژن O (سوماتیک): نشاندهنده عفونت حاد
- آنتیژن H (تاژکی): نشاندهنده عفونت مزمن یا ایمنی
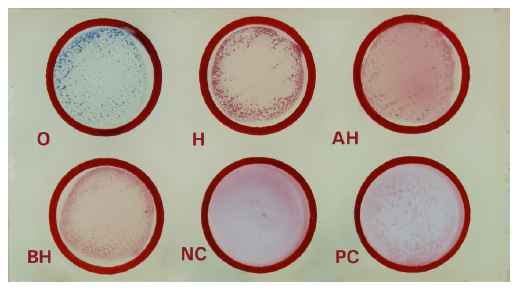
روش انجام آزمایش ویدال
جهت مطالعه ی جانع در مورد روش انجام آزمایش ویدال به لینک زیر مراجعه کنید:
روش انجام تست ویدال: راهنمای جامع انجام، کنترل کیفی و تفسیر نتایج برای کارشناسان آزمایشگاه
مقایسه تفاوتهای اصلی بین تست رایت و ویدال (جدول مقایسهای)
| ویژگیها | تست رایت (Wright) | تست ویدال (Widal) |
|---|---|---|
| بیماری مورد بررسی | بروسلوز (تب مالت) | تب تیفوئید و پاراتیفوئید |
| عامل بیماریزا | Brucella abortus, B. melitensis | Salmonella typhi, S. paratyphi |
| نوع آنتیژن | آنتیژن کشتهشده بروسلا | آنتیژنهای O و H سالمونلا |
| نوع آنتیبادی | IgM و IgG ضد بروسلا | IgM و IgG ضد سالمونلا |
| روش انجام | آگلوتیناسیون لولهای (Tube) | آگلوتیناسیون لولهای (Tube) |
| مدت انکوباسیون | ۲۴ ساعت در ۳۷°C | ۲ ساعت در ۳۷°C |
| تیتر مثبت معمول | ≥ 1:160 (معمولاً) | ≥ 1:160 برای O یا H (وابسته به منطقه) |
| نمونهٔ مورد استفاده | سرم بیمار | سرم بیمار |
| کاربرد بالینی | تشخیص و پیگیری درمان بروسلوز | تشخیص اولیه تب تیفوئید |
| مثبت کاذب محتمل | بیماریهای مزمن/واکنش متقاطع | واکسیناسیون/عفونت قبلی سالمونلا |
تفسیر نتایج در دو تست
✅ تست رایت
- < 1:80: منفی
- 1:80 تا 1:160: مشکوک (تکرار)
- ≥ 1:160: مثبت (عفونت فعال یا اخیر)
- افزایش چهاربرابری تیتر در دو نمونهٔ با فاصله دو هفته: نشانهٔ عفونت فعال
✅ تست ویدال
- آنتیژن O مثبت: عفونت حاد
- آنتیژن H مثبت: عفونت مزمن/پس از واکسیناسیون
- Vi (در بعضی کیتها): عفونت فعال تیفوئید
شباهتهای تست رایت و ویدال
- هر دو بر اساس واکنش آگلوتیناسیون انجام میشوند.
- در هر دو از سرم بیمار و آنتیژن کشتهشده استفاده میشود.
- هر دو تست نیمهکمی هستند و تیتر آنتیبادی گزارش میشود.
- هر دو در تشخیص بیماریهای باکتریایی مرتبط با حیوان/آب آلوده نقش دارند.
تفاوت در خطاها و محدودیتها
| نوع خطا | تست رایت | تست ویدال |
|---|---|---|
| خطای نمونهگیری | آلودگی یا همولیز سرم | آلودگی یا نگهداری نادرست |
| نتایج مثبت کاذب | تماس با بروسلاهای غیرپاتوژن/متقاطع | واکسیناسیون یا تماس قبلی با سالمونلا |
| تأثیر آنتیبیوتیکها | کاهش تیتر در درمان | کاهش تیتر پس از شروع درمان |
| نیاز به کنترل کیفی | دارد (کنترل مثبت/منفی) | دارد (O و H کنترل مثبت) |
نکات مهم برای آزمایشگاهها
- در هر دو تست، کنترل کیفی داخلی (QC) باید قبل از انجام نمونه بیماران انجام شود.
- آنتیژنها باید در دمای ۲–۸ درجه سانتیگراد نگهداری شوند.
- برای تفسیر نتایج باید پیشینه اپیدمیولوژیک منطقه در نظر گرفته شود.
- توصیه میشود تست دوم با فاصله ۱۰ تا ۱۴ روز انجام شود تا افزایش تیتر بررسی گردد.
حساسیت و ویژگی (Sensitivity/Specificity)
حساسیت و ویژگی هر دو تست به زمان نمونهگیری، پیشزمینه واکسیناسیون/عفونت قبلی و کیفیت آنتیژن وابسته است. در مناطق اندمیک، تکیهٔ صرف بر یک تیتر قطع میتواند منجر به مثبت کاذب شود؛ لذا تأکید بر افزایش چهاربرابری تیتر در نمونههای paired توصیه میگردد.
جایگزینها و تستهای تکمیلی
- برای بروسلوز: ELISA IgM/IgG، کشت خون/مغز استخوان، PCR
- برای تیفوئید: کشت خون/مدفوع، آنتیژنهای اختصاصی رپید، PCR
کیفیت معرف و حملونقل
آنتیژنهای بروسلا و سالمونلا باید در زنجیرهٔ سرد ۲–۸°C نگهداری و در برابر نور مستقیم محافظت شوند. یخزدگی و یخگشاییهای مکرر میتواند قدرت آگلوتیناسیون را کاهش دهد.
تداخلها
روماتوئید فاکتور بالا، همولیز شدید، لیپمیک بودن سرم و آلودگی میتواند در خوانشها اختلال ایجاد کند. استفاده از کنترل منفی در هر سری آزمایش الزامی است.
جمعبندی تفاوت تست رایت و ویدال
تست رایت و ویدال از نظر اصول سرولوژیک مشابهاند، اما کاربرد آنها کاملاً متفاوت است.
تست رایت برای تشخیص بروسلوز (Brucellosis) و تست ویدال برای تب تیفوئید (Typhoid) استفاده میشود.
با وجود سادگی این آزمایشها، تفسیر دقیق نتایج و کنترل کیفی صحیح نقش مهمی در جلوگیری از خطاهای تشخیصی دارد.
سؤالات رایج درباره تفاوت تست رایت و ویدال
۱) اصلیترین تفاوت تست رایت و ویدال چیست؟
رایت برای بروسلوز با آنتیژن بروسلا و انکوباسیون ۲۴ ساعته است؛ ویدال برای تیفوئید با آنتیژنهای O/H سالمونلا و معمولاً ۲ ساعت.
۲) تیتر مثبت در هر تست چقدر است؟
رایت معمولاً ≥ 1:160؛ ویدال بسته به منطقه برای O یا H معمولاً ≥ 1:160.
۳) آیا هر دو تست نیاز به کنترل کیفی دارند؟
بله؛ کنترل مثبت و منفی برای تضمین صحت نتایج ضروری است.
۴) کدام تست برای فاز حاد مناسبتر است؟
در ویدال، آنتیژن O نماینده فاز حاد است؛ در رایت افزایش چهاربرابری تیتر نشانهٔ عفونت فعال است.
۵) شایعترین علت مثبت کاذب در ویدال چیست؟
واکسیناسیون یا تماس قبلی با سالمونلا.
۶) شایعترین منبع خطا در رایت چیست؟
خطای رقتسازی و نگهداری نامناسب آنتیژنها.
۷) در مناطق اندمیک، تفسیر چگونه باشد؟
به سابقهٔ منطقهای و تغییر تیتر در نمونههای paired تکیه کنید، نه فقط یک عدد قطع.
۸) چه تستهایی برای تأیید نتایج پیشنهاد میشود؟
برای بروسلوز: ELISA/کشت/PCR؛ برای تیفوئید: کشت خون/مدفوع و تستهای مولکولی.
۹) آیا شروع آنتیبیوتیکها روی تیتر اثر دارد؟
بله؛ ممکن است تیتر کاهش یابد و تفسیر را دشوار کند.
۱۰) نمونهٔ مناسب چیست و چگونه نگهداری شود؟
سرم؛ جداسازی بهموقع، نگهداری ۲–۸°C کوتاهمدت یا -20°C بلندمدت.
منابع معتبر برای مطالعه بیشتر در مورد تفاوت تست رایت و ویدال
- https://pmc.ncbi.nlm.nih.gov/articles/PMC6860005/
- Henry’s Clinical Diagnosis and Management by Laboratory Methods, 24th Edition.
